CARBOHIDRATOS
¿Qué es un carbohidrato?
Un carbohidrato es un polihidroxialdehído o una polihidroxicetona o una substancia que al hidrolizarse produce uno de éstos.
El origen del nombre "carbohidrato" surge del hecho de que muchas de las substancias de esta clase tienen formulas empíricas que sugieren que hay carbonos "hidratados", en los que la razón de átomos de carbono a hidrógeno a oxígeno es de 1:2:1. Por ejemplo, la formula empírica de D-Glucosa es C6H12O6, que también puede escribirse como (CH2O)6 ó C6(H2O)6. Sin embargo, aunque muchos carbohidratos se conforman a esta formula empírica (CH2O)n, muchos otros no responden a la misma y otros contienen nitrógeno, fósforo o azúfre.
¿Cuántas clases de carbohidratos existen?
Hay tres principales clases de carbohidratos: monosacáridos, oligosacáridos y polisacáridos. El término "sacárido" viene de la palabra griega 'sakkharon' que significa azúcar (en latín 'saccharum').
Los monosacáridos son la azúcares simples, es decir, aquellas que contienen una sola unidad polihidroxialdehídica o cetónica. El monosacárido más abundante en la naturaleza es D-glucosa, azúcar de seis carbonos.
Si el monosacárido es un polihidroxialdehído, se clasifica como una aldosa; si es una polihidroxicetona, entonces es una cetosa. Los monosacáridos mas simples contienen tres carbonos: las triosas gliceraldehído (aldosa) y dihidroxiacetona (cetosa). Monosacáridos de 4, 5, 6 y 7 carbonos se conocen como tetrosas pentosas, hexosas y heptosas, respectivamente. Cada una de éstas existe en dos series: aldotetrosas y cetotrosas, aldopentosas y cetopentosas, aldohexosas y cetohexosas, etc.
Los oligosacáridos (del griego "oligos", pocos) consisten de cortas cadenas de unidades de monosacáridos unidas entre sí por enlaces covalentes. De éstos, los más abundantes son los disacáridos , que contienen dos unidades monosacáridas. Ejemplo típico es sacarosa, o azúcar de la caña.
Muchos oligosacáridos de tres o más unidades no se encuentran en forma libre sino unidas a cadenas polipéptidas laterales en las glicoproteínas.
Los polisacáridos consisten de largas cadenas conteniendo cientos o miles de unidades monosacáridas. En esta clasifica- ción están celulosa, glucógeno y almidón.
¿Exhiben quiralidad los carbohidratos?
Sí, todos los monosacáridos, excepto dihidroxiacetona, contienen uno a más centros quirales, por lo que se encuentran en formas isoméricas ópticamente activas. Gliceraldehído, la aldosa más simple, contiene un sólo centro quiral, por lo que existe como un par de enantiómeros:
El D-Gliceraldehído (configuración R) tiene el grupo -OH en el carbono quiral hacia la derecha; L-Gliceraldehído (configuración S) lo tiene hacia la izquierda. Todos lo estereoisómeros de los monosacáridos están relacionados a este estándar, por lo que los prefijos D- y L- se usan para referirse a la configuración del carbono quiral más distante del carbonilo. Por ejemplo:

¿Qué son epímeros?
Cuando dos azúcares difieren sólo en la configuración de uno de sus átomos de carbono se dice que son azúcares epímeras. Los epímeros son, pués, diasterómeros. Por ejemplo D-Glucosa y D-Manosa son epímeras con respecto al carbono 2, mientras que D-Glucosa y D-Galactosa lo son con respecto al carbono 4:

¿Qué tipo de estructura exhiben los monosacáridos?
Aunque se presentan las estructuras en forma de cadena recta, lo cierto es que ésto sólo es correcto para las triosas y tetrosas.
Por lo general, monosacáridos con cinco o más carbonos se encuentran en solución como estructuras cíclicas en las que el grupo carbonilo no está "libre" sino que forma un enlace covalente con un grupo -OH de la cadena. El nuevo enlace genera un hemiacetal, lo que convierte el carbono del carbonilo en un nuevo centro quiral.
El monosacárido cíclico existe, entonces, como dos estereoisómeros diferentes, llamados anómeros y designados con las letras  (alfa) y ß (beta).
(alfa) y ß (beta).

¿Qué es un hemiacetal?
La formación de un hemiacetal surge de la reacción de un grupo carbonilo con un alcohol, como se ilustra a continuación:

Por enlazar cuatro grupos diferentes, el carbono del hemiacetal es quiral. Este carbono es el carbono del carbonilo en el aldehído.La formación del nuevo centro quiral genera un par de estereoisómeros.
En la química de los carbohidratos, el nuevo carbono quiral de denomina carbono anomérico porque genera dos anómeros: diasterómeros que son epímeros en el carbono hemiacetálico.
Por ejemplo, D-Glucosa produce los anómeros alfa-D-Glucopiranosa y ß-D-Glucopiranosa:

Se ha establecido que los grupos que están orientados hacia la derecha en la estructura de cadena recta se dibujen hacia abajo en la estructura cíclica; los que están hacia la izquierda en la cadena recta, en la cíclica se dibujan hacia arriba.
Loa anómeros son, pués, formas isoméricas de un monosacárido que difieren en la configuración del carbono hemiacetálico.
¿Por qué a los anómeros de D-Glucosa se les da el nombre de piranosa?
Loa anómeros de D-Glucosa se les da el nombre de piranosa porque la estructura del hemiacetal cíclico se asemeja a pirano, un compuesto heterocíclico con seis miembros en el anillo:

(Cabe señalar que en la formación de los anómeros de D- Glucosa también se forman hemiacetes cíclicos de cinco miembros en el anillo, pero éstos son menos estables que los anómeros de seis miembros y se producen solo en trazas.)
¿Qué propiedades exhiben los anómeros?
Por ser diasterómeros, los anómeros exhiben diferentes propiedades físicas. Por ejemplo, la rotación específica del anómero alfa es [ ] = + 112.2°; la del anómero ß es [
] = + 112.2°; la del anómero ß es [ ] = + 18.7°. Los puntos de fusión son de 146°C para el primero y 148-155°C para el último, lo que implica que cada anómero existe independiente del otro. De hecho, ambos se pueden aislar como sólidos cristalinos puros. Ambos exhiben,también, mutarrotación.
] = + 18.7°. Los puntos de fusión son de 146°C para el primero y 148-155°C para el último, lo que implica que cada anómero existe independiente del otro. De hecho, ambos se pueden aislar como sólidos cristalinos puros. Ambos exhiben,también, mutarrotación.
¿Qué es la mutarrotación?
La mutarrotación es el cambio espontáneo en la rotación óptica de una solución fresca de un estereoisómero puro. Esta es causada por la epimerización o algún otro cambio estructural. Por lo general, el valor de equilibrio de la rotación no es cero.
En el caso de la mutarrotación de los anómeros de D-Glucosa, la solución tiene un valor de rotación específica de +52.5°.
La mezcla en equilibrio es de un 36% del anómero alfa a un 64% del beta. El equilibrio entre ambos anómeros se produce a través de la estructura de cadena abierta (aldehído libre), como se ilustra a continuación:

(Sólo se producen trazas de los anómeros  y ß glucofuranosa)
y ß glucofuranosa)
¿Por qué en la mezcla en equlibrio hay una mayor proporción del anómero ß?
El anómero ß se produce en mayor proporción por que es más estable. Básicamente, la estabilidad se debe a que tanto el grupo -OH del carbono anomérico, como los demas substituyentes en los otros carbonos, están todos en posición ecuatorial en el anómero ß, mintras que en el  está en posición axial el -OH del carbono hemiacetálico:
está en posición axial el -OH del carbono hemiacetálico:

¿Forman las cetosas hemiacetales cíclicos?
Sí; la cetosas de cinco o más carbonos producen hemiacetales cíclicos, formando también anómeros  y ß. Por ejemplo, la fructosa es una cetohexosa que genera un hemiacetal cíclico combinando el carbonilo, que está en el cabono 2, con el grupo -OH del carbono 5:
y ß. Por ejemplo, la fructosa es una cetohexosa que genera un hemiacetal cíclico combinando el carbonilo, que está en el cabono 2, con el grupo -OH del carbono 5:

Las estructuras de Haworth de los anómeros representan anillos de cinco miembros, como se ilustra a continuación :

¿Por que se le da el nombre de furanosa?
El nombre de furanosa viene por la semejanza de estas estructuras con furano, un compuesto heterocíclico de cinco miembros en el anillo:

¿Produce la D-Fructosa, además de las fructofuranosas, hemiacetales de seis miembros o fructopiranosas?
Sí; así como la glucosa produce hemiacetales de cinco miembros (glucofuranosas), la fructosa también genera fructopiranosas anoméricas:

¿Exhibe mutarrotación la D-Fructosa?
Sí; la mutarrotación es una característica de todos las azúcares que generan anómeros. En el caso de D-Fructosa, la mutarrotación es algo más compleja que para D-Glucosa. De hecho, la única forma cristalina de fructosa es la ß-D-fructopiranosa, cuya rotación específica es de -133.5°. Al disolverse, mutarrota rápidamente hasta alcanzar el valor de equilibrio de -92°.
Esta mutarrotación involucra no tan sólo la isomerización entre los anómeros alfa y ß-piranosa, sino que también genera la formación de los anómeros alfa y ß-furanosa.
El siguiente diagrama ilustra el proceso de mutarrotación de la D-Fructosa, incluyendo el porcentaje (%) en equilibrio de cada isómero:

¿Si la forma cristalina de fructosa es el anómero ß piranosa, porque es importante la fructofuranosa?
La cristalización de D-Fructosa produce el anómero ß-Fructopiranosa en forma pura, sin embargo el isómero de furanosa es importante porque tanto en sacarosa como en muchos oligosacáridos, la fructosa aparece en forma de fructofuranosa.
¿Puede darse una interconversión entre Glucosa y Fructosa?
Sí, la interconversión entre Glucosa y Fructosa puede darse mediante una isomerización catalizada por bases (o por enzimas). La tranformación se da via un enediol :

¿Cómo son las estructuras de los disacáridos?
Los disacáridos son carbohidratos que contienen dos unidades monosacáridas unidas entre sí por un enlace covalente. En muchos el enlace químico que une ambas estructuras se conoce como un enlace glucosídico, formado por la reacción entre el grupo -OH de uno de los monosacáridos con el carbono anomérico del otro monosacárido.
El enlace glucosídico es el equivalente de un acetal:

Los enlaces glucosídicos son resistentes a las bases pero sufren hidrólisis ácida. De aquí que los disacáridos pueden hidrolizarse para producir sus correspondiente monosacáridos al calentarse en solución ácida acuosa.
Como se indicó, el enlace glucosídico se da entre el carbono anomérico de una azúcar con el grupo -OH de la otra. La configuración del enlace glucosídico va a estar dada, entonces, por el carbono anomérico. Este, según se explicó, se denomina como  o ß , dependiendo si el -OH se orienta hacia abajo o hacia arriba, respectivamente.
o ß , dependiendo si el -OH se orienta hacia abajo o hacia arriba, respectivamente.
Por ejemplo, en una piranosa, los anómeros serán:

Si estos reaccionaran con el grupo -OH del carbono 4 de otra piranosa entonces se formaria un enlace glucosídico entre ambos y, por ende, un disacárido:
Formación de un disacárido via enlace glucosídico:

Como el enlace se produjo entre el carbono anomérico (1), de configuración, con el el grupo -OH del carbono 4 , el enlace se denomina  (1 ---> 4'), y el compuesto se conoce como un glucósido.
(1 ---> 4'), y el compuesto se conoce como un glucósido.
Para el anómero ß:

Como el enlace se produjo entre el carbono anomérico (1), de configuración ß, con el el grupo -OH del carbono 4 , el enlace se denomina ß (1 --- > 4), y el compuesto se conoce, también como un glucósido.
Otra forma de ilustrar el enlace ß glucosídico es la siguiente:

¿Cuáles son los disacáridos más comunes?
Los disacáridos más comunes son maltosa, lactosa y sacarosa.
MALTOSA es un disacárido de glucosa, unidas entre sí por un enlace glicosídico  (1 ---> 4). La maltosa es el azúcar de la malta que es la cebada germinada (o también centeno y trigo). Su uso es mayormente para eleborar cerveza, alcohol, o extracto de malta. Su nombre sistémico es:
4-O-(
(1 ---> 4). La maltosa es el azúcar de la malta que es la cebada germinada (o también centeno y trigo). Su uso es mayormente para eleborar cerveza, alcohol, o extracto de malta. Su nombre sistémico es:
4-O-( -D-glucopiranosil)-D-glucopiranosa
-D-glucopiranosil)-D-glucopiranosa
Su estructura es la siguiente:

LACTOSA es un disacárido de glucosa y galactosa unidas entre sí por un enlace glicosídico ß (1 ---> 4). Es el azúcar de la leche. El enlace se produce entre el carbono anomérico de la galactosa con el -OH del carbono 4 de la glucosa, por lo que es una glucopiranosa substituída. Su nombre sistémico es:
4-O-(ß -D-galactopiranosil)-D-glucopiranosa
Su estructura es la siguiente:

SACAROSA es un disacárido de glucosa y fructosa. Es el azúcar de la caña. El enlace glucosídico es muy particular porque se produce entre el carbono anomérico del anómero  de glucosa con el carbono anomérico del anómero ß-furanósido de fructosa, es decir, entre el carbono 1 de glucosa y el carbono 2 de fructosa.
de glucosa con el carbono anomérico del anómero ß-furanósido de fructosa, es decir, entre el carbono 1 de glucosa y el carbono 2 de fructosa.
Su nombre sistémico es:
O- -D-glucopiranosil)-(1 ---> 2)-ß-D-fructofuranósido
-D-glucopiranosil)-(1 ---> 2)-ß-D-fructofuranósido
También puede llamarse:
( -D-glucopiranosil)-ß-D-fructofuranósido
-D-glucopiranosil)-ß-D-fructofuranósido
o bién:
(ß-D-fructofuranosil)- -D-glucopiranósido
-D-glucopiranósido
Su estructura es la siguiente:

¿Cuáles son algunos de los polisacáridos más comunes?
Los polisacáridos son muy abundantes en la naturaleza. Los hay de estructura estrictamente lineal como ramificados. Ejemplos clásicos son los siguientes:
CELULOSA: es el compuesto orgánico más abundante de la naturaleza pues se encuentra en todo material vegetal. Su función principal es la del dar soporte estructural a las plantas. Es un polisacárido lineal de glucosa, unidas entre sí por enlaces glucosídicos ß(1 ---> 4):

La celulosa no puede ser digerida por los seres humanos por carecer éstos de la enzima apropiada para hidrolizar el enlace ß glucosídico. Los rumiantes, por su parte, tienen en su estómago bacterias que poseen la debidas enzimas para este proceso.
ALMIDON: es la forma en que las plantas almacenan su reserva de carbohidratos. Como la celulosa, es un polisacárido de glucosa. Difiere, sin embargo, en dos aspectos: (1) es una mezcla de dos moléculas, amilosa (10-20%) y amilopectina (80-90%) (2) las unidades de glucosa están enlazadas entre sí por enlaces glucosídicos.
Por otro lado, los dos polimeros que constituyen el almidón son estructuralmente diferentes: la amilosa es un polímero lineal similar a la celulosa, excepto que el enlace glucosídico es  (1 ---> 4).
(1 ---> 4).
Amilosa forma un complejo con yodo de color azul intenso. Su estructura es la siguiente:

La cadena de glucosas en amilosa se enrolla en una estructura en forma de espiral:

AMILOPECTINA: es similar a la amilosa, pero es un polímero con ramificaciones cada 20 a 25 glucosas. En estas ramificaciones se produce un enlace  (1 ---> 6) con otra cadena de glucosa unidas por enlaces
(1 ---> 6) con otra cadena de glucosa unidas por enlaces  (1 ---> 4):
(1 ---> 4):

GLUCOGENO: es la variedad de almacenamiento de carbohidratos en la célula animal. Es similar a la estructura de amilopectina, excepto que es más ramificada y más compacta. Las ramificaciones se dan cada 10 a 12 unidades de glucosa.
QUITINA: es un polisacárido que se encuentra en el carapacho de las langostas y los cangrejos y en el esqueleto externo de insectos y arañas. La unidad que se repite en este polisacárido es N-acetilglucosamina, y el enlace glucosídico es ß (1---4). Su estructura es similar a la de celulosa, como se ilustra a continuación:

HEPARINA: es un polisacárido sulfatado que consiste predominantemente de unidades alternas de 2-sulfato de D-glucuronato y 6-sulfato de N-sulfo-D-glucosamina. La heparina se encuentra en células de las paredes arteriales; cuando hay una lesión, ésta se libera para inhibir la coagulación de la sangre y de esta forma evitar la formación de coágulos libres. Su estructura parcial se presenta a continuación:

¿Qué compuestos contienen carbohidratos?
Existen un sinnúmero de compuestos que contienen carbohidra tos como parte de sus estructuras. A continuación se presentan algunos ejemplos:
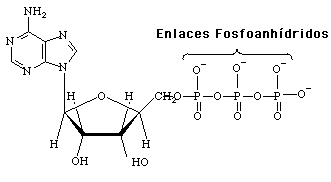
1- Trifosfáto de adenosina, mejor conocida por las siglas "ATP" (Adenosine triphosphate), es el principal compuesto en el que se transforma la energía liberada en las oxidaciones biológicas. Su estructura contiene, además de Adenina y el trifosfáto, el monosacárido D- Ribosa, una aldopentosa en forma de furanosa. La estructura de "ATP" se ilustra a continuación:
2- Salicina: este es un compuesto que se encuentra en la corteza del árbol de sauce. Antiguamente se usaba como remedio para el dolor debido al efecto analgésico de la Salicina. De hecho, de este glucósido se puede conseguir ácido salicílico,
precursor del ácido acetilsalicílico, mejor conocido como aspirina.

3-Estreptomicina: es un antibiótico constituído por los siguien tes componentes: la amino azúcar L-glucosa, el monosacárido estreptosa, y estreptidina, un derivado de ciclohexano llamado amino ciclitol. La estructura de este antibiótico, descubierto en 1944, es la siguiente:

3-Nucleosidos obtenidos del ADN y ARN: tanto el ácido-2-desoxiribonucléico, ADN (2-deoxyribonucleic acid: DNA), como el ribonucléico,ARN (o RNA), contienen una aldopentosa en forma de furanosa: 2-desoxi-D-Ribosa y D-Ribosa, respectivamente.

¿Qué es azúcar invertida?
La hidrólisis de Sacarosa produce 1 equivalente de glucosa y 1 equivalente de fructosa. Esta mezcla de 1:1 es lo que se conoce como azúcar invertida. Se designa como invertida por que el signo de la rotación específica de sacarosa ( = +65.5°) cambia (se invierte) por su hidrólisis a la mezcla glucosa/ fructosa: = -22°. Las abejas, por ejemplo, contienen la enzima invertasa que cataliza la hidrólisis de sacarosa a glucosa + fructosa.
¿Cómo comparan la azúcares en dulzura?
Sacarosa es el estándar que se usa para medir la dulcedumbre o dulzura relativa entre carbohidratos, y se le asigna un valor de 100. La siguiente tabla ilustra esta relación con algunos carbohidratos y dos endulzadores artificiales: Sacarina y Aspartama.
Azúcar - [Dulcedumbre Relativa]
- Sacarosa - [100] (*Estándar)
- Fructosa - [170]
- Glucosa - [70]
- Maltosa - [30]
- Lactosa - [16]
- Sacarina - [40,000]
- Aspartama - [20,000]
De la tabla se infiere que la fructosa es 1.7 veces más dulce que sacarosa, mientras que el endulzador artificial Sacarina es 400 veces más dulce. Sin embargo, sacarina no tiene ningún valor nutricional y se considera como un carcinógeno potencial.
Aspartama, por su parte, es 200 veces más dulce que sacarosa, y ha substituído a la sacarina como endulzador artificial. Aunque es un derivado de aminoácidos, tampoco tiene valor nutritivo. Esto implica que, por no ser carbohidratos, no entran al proceso metabólico normal de éstos. La estructura química de ambos se presenta a continuación:



 (alfa) y ß (beta).
(alfa) y ß (beta).




























