
Además del componente proteínico (apoenzima), algunas enzimas requieren de otras entidades químicas no proteicas, denominados grupos prostéticos. El grupo prostético define lo que se conoce como cofactor o coenzima, que son necesarios para que la enzima pueda funcionar adecuadamente.La combinación de la apoenzima con el grupo prostético se denomina holoenzima.
Un cofactor o coenzima puede ser una molécula orgánica u organometálica, o un metal iónico. Así, el grupo prostético es un cofactor o una coenzima enlazada covalentemente a la enzima (si lo hace por atracciones no-covalentes, está firmemente unida a la enzima).
Otras coenzimas se unen debilmente a la enzima (por enlaces no-covalentes), por lo que la unión es temporal: sólo durante el proceso de reacción.
Cada coenzima lleva a cabo una función particular; también, la actividad catalítica se regula por medio de las coenzimas.
Muchas coenzimas son derivados de una vitamina. Las vitaminas son esenciales para el crecimiento y desarrollo adecuado y pueden ser acuosolubles o liposolubles. Las liposolubles son las denominadas vitaminas A , D , E y K.

La ingestión de grandes cantidades de estas vitaminas puede ser dañino porque se acumulan en el tejido graso y en las membranas.
La siguientes figuras ilustran las vitaminas acuosolubles que sirven como precursoras de coenzimas:




IONES METALICOS COMO COENZIMAS O COFACTORES
Ls iones de los metales de transición (Mg2+, Mn2+, Cu2+ Zn2+, Fe2+, Fe3+, Ni2+ y Mo4+ o Mo6+,son requeridos como cofactores para la acción enzimática de algunas enzimas.

Estos se requieren sólo en pequeñas cantidades, por lo que se consideran como elementos esenciales en trazas o micronutrientes.
Ejemplos:
A- Dinucleotidos de adenina y nicotinamida (NAD) y de adenina y nicotinamida fosfáto (NADP)
Hay dos formas de coenzimas para ácido nicotínico: el dinucleotido de adenina y nicotinamida (NAD) y el dinucleotido de adenina y nicotinamida fosfáto (NADP). Estas coensimas existen en estado oxidado (NAD+ y NADP+) y reducido (NADH y NADPH). La reducción se produce cuando se añade H2 y la oxidación cuando se remueve H2. Esta adición o remoción de H2 puede visualizarse como la de dos átomos de hidrógeno (H. + H.) o dos protones y dos electrones (2H+ + 2e-) o un ion hidruro y un protón (H:- + H+ ).
Tanto el NAD+ como el NADP+ contienen adenosina y el derivado N-ribosil de nicotinamida.

La estructura de NAD+(y la de NADP+) se ilustra en la siguiente figura:

Ambos, NAD+ y NADP+, transportan electrones para una serie de enzimas del grupo denominado deshidrogenasas: enzimas que catalizan reacciones de oxidación-reducción y reacciones de remoción de hidrógeno. Muchas de las deshidrogenasas que catalizan reacciones involucradas en la generación de energía usan NADH como coenzima. Las enzimas que requieren de NADPH usualmente catalizan reacciones de biosíntesis. Un reducido número de deshidrogenasas pueden usar NADH o NADPH.
La alcohol deshidrogenasa cataliza la oxidación reversible de etanol para formar acetaldehído:
CH3CH2OH + NAD+ <=====> CH3CHO + NADH + H+
El NAD+ acepta un ion hidruro del alcohol, que se oxida a nivel de aldehído. Un H+ se libera al final: el resultado es la remoción de un ion hidruro y un protón (H:- + H+ ), o sea, una oxidación:
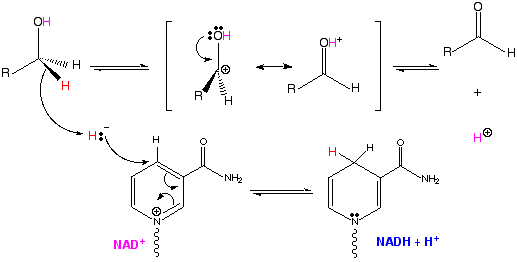
En muchas de las reacciones catalizadas por deshidrogenasas el NAD+ (o NADP+) se une a la enzima sólo en forma transitoria. Luego de que la versión reducida de la coenzima (NADH o NADPH) se libera de la enzima le dona el ion hidruro a otra molécula, llamada receptor de electrones. El enlace de alta energía entre el hidrógeno y el anillo de nicotinamida proveen la energía para la transferencia del ion hidruro.
B-Monoucleotido de flavina (FMN) y dinucleotido de flavina adenina (FAD)
Riboflavina (vitamina B12) es un componente de dos coenzimas: monoucleotido de flavina (FMN) y dinucleotido de flavina adenina (FAD):

Ambas funcionan como grupos prostéticos fuertemente unidos en un tipo de enzimas conocidas como flavoproteínas, que catalizan diversas reacciones de oxidación reducción: funcionan como deshidrogenasas, oxidasas e hidroxilasas. El grupo isoaloxazino actúa como donante o aceptador de de dos átomos de hidrógeno (H.):
