CARACTERISTICAS DE LAS REACCIONES ORGANICAS
¿Qué son los reactantes en una reacción?
Los reactantes son aquellos compuestos que se van combinar para generar un producto diferente a ellos. El compuesto orgánico que sufre un cambio estructural o de grupo funcional se denomina el substrato.

¿Cómo pueden clasificarse los reactantes en una reacción?
La mayor parte de la reacciones orgánicas pueden considerarse como ionicas ya que los reactantes o son ricos en electrones o son deficientes en los mismos. Así, aquellos que son ricos en electrones los clasificamos como nucleófilos; aquellos que son deficientes en electrones se conocen como electrófilo.
Típicamente, los nucleófilos son eléctricamente neutros o poseen carga negativa (aniones) mientras que los electrófilos son eléctricamente neutros o poseen una carga positiva (cationes).
En una reacción ionica el nucleófilo (Nu:) comparte un par de electrones con un electrófilo (E) en el proceso de formación de enlaces:

Los nucleófilos son bases de Lewis porque son donantes de electrones; los electrófilos son, a su vez, ácidos de Lewis porque aceptan pares electrónicos.
Cuando dos moléculas o iones reaccionan, uno debe actuar como nucleófilo y el otro como electrófilo. Sin embargo, esta designación se convierte en arbitraria en aquellas reacciones en que ambos reactantes son compuestos orgánicos. Muchas transformaciones proceden en dos o más pasos, lo que implica que hay que determinar cuál de estos pasos servirá de base para clasificar los reactantes.
La clasificación de una reacción que ocurre entre los grupos funcionales de dos moléculas orgánicas está basada en las características de cada molécula y, muchas veces, de las condiciones de reacción
¿Qué es un grupo funcional?
Un grupo funcional es el átomo o el grupos de átomos responsable de la reactividad de una molécula, bajo las condiciones dadas.
¿Cómo se clasifica una reacción orgánica?
Una reacción orgánica puede clasificarse usando uno de dos criterios:
(a) por el tipo de operación que se lleva a cabo; y
(b) por el carácter electrónico de los reactantes.
Al clasificar una reacción orgánica por el tipo de operación, ésta puede designarse como adición, eliminación o substitución. Cada clasificación operacional puede combinarse con una clasificación electrónica para describir la totalidad del mecanismo de reacción. Por ejemplo, una adición puede clasificarse como nucleofílica o electrofílica.
¿Qué es una reacción de adición?
Una reacción de adición ocurre en compuestos insaturados (que contienen dobles o triples enlaces). Estas moléculas son capaces de aceptar un átomo o grupos adicionales sin exceder la covalencia de sus propios átomos. Ejemplos son la Hidrogenación (adición de hidrógeno), la Hidratación (adición de agua) y la Hidrohalogenación (adición de HX):

¿Qué es una reacción de eliminación?
Una eliminación es lo contrario a una adición. En este caso, se remueven átomos de una molécula para formar productos con enlaces múltiples o, en algunos casos, anillos. En este tipo de reacción, átomos originalmente saturados se convierten en insaturados. La reacción de eliminación más común es la eliminación 1,2 , en la que los átomos o grupos removidos se encuentran en átomos adyacentes. Por ejemplo:
Deshidratación (eliminación de agua), Deshidrohalogenación (eliminación de halogenuro de hidrógeno, HX) y Deshidrogenación (eliminación de hidrógeno, H2)

Qué es una reacción se substitución?
Las reacciones de substitución ocurren cuando un átomo o grupo suplidos por el reactivo reponen un átomo o grupo en la molécula del substrato. Esta reacción puede ocurrir tanto en carbonos saturados como insaturados. Por ejemplo:

¿Qué es un mecanismo de reacción?
Un mecanismo de reacción es la descripción, paso a paso, del curso de una reacción según los reactantes se convierten a productos. Esta descripción incluye, entre otros, los movimientos electrónicos por los que se forman o se rompen enlaces, la generación de intermediarios, las relaciones espaciales de los átomos según se lleva a cabo la transformación, así como los cambios energéticos que ocurren en cada etapa de la reacción.
Todo mecanismo propuesto para una reacción dada responde a los datos experimentales disponibles. Por eso, lo que se propone es lo "más razonable" dentro de ese contexto, ya que para una misma reacción se pueden establecer varios mecanismos.
¿Cómo se propone un mecanismo de reacción?
Se sabe que para la mayor parte de las reacciones orgánicas se pueden concebir muchos mecanismos. A pesar de que la decisión para determinar el mecanismo más razonable está mayormente condicionada a la experiencia o a la intuición, se pueden apuntar algunas reglas básicas que ayudan a establecer la "razonabilidad" del mismo:
1. El mecanismo debe ser lo más simple posible, sin dejar de ser detallado, es decir, que explique todos los hechos disponibles.
2. Las reacciones pueden dividirse arbitrariamente en dos categorías:
-reacciones concertadas, que ocurren en un sólo paso
-reacciones no-concertadas, que ocurren en más de un paso (multipasos)
En cada categoría, cada paso individual (elemental) debe ser o unimolecular (involucra una reacción de una sola molécula) o bimolecular (involucra la interacción de dos moléculas).
3. Las reacciones no-concertadas (multipasos) tienen una necesaria consecuencia: intermediarios reactivos.
4. Los pasos deben ser energeticamente plausibles y quimicamente razonables
La comprensión de un mecanismo de reacción necesariamente comienza con el conocimiento del tipo de reacción. Esto es, debe establecerse bien la estructura de los materiales iniciales y debe determinarse bien la estructura de los productos.
No se puede proponer mecanismo alguno si no se está cierto de como inicia y finaliza una reacción dada.
¿Qué implica el movimiento de electrones en un mecanismo de reacción?
Una reacción química es una secuencia de ruptura y formación de enlaces que involucran electrones de enlace y no-enlace. El mecanismo de reacción tiene que tomar en cuanta estos movimientos.
Es práctica común reseñar el movimiento de electrones con unas flechas curvas, indicando el movimiento desde la fuente de electrones hacia el receptor de los mismos, es decir, del nucleófilo al electrófilo:

También se usan las flechas para ilustrar el movimiento electrónico dentro de una molécula. Por ejemplo:

En la ruptura heterolitica de un enlace covalente, el par de electrones del enlace se quedan en uno de los dos fragmentos, formando un anión; el otro fragmento queda como un catión:

En la ruptura homolítica de un enlace, cada fragmento retiene uno de los dos electrones del enlace (el movimiento de un electrón para cada porción se ilustra con flechas con medio cabezal ). El producto de este proceso es un radical :

La unión de dos radicales se ilustra así:

¿Qué es un intermediario reactivo?
Un intermediario reactivo es una especie inestable y de corta vida que se forma en el curso de la reacción de reactantes a productos. Estas especies no se pueden aislar y son sumamente reactivas.
Hay cuatro intermediarios reactivos que comunmente se generan en las reacciones orgánicas: carbanión, carbocatión , carbeno y radical.
¿Qué es un carbanión?
Un carbanión es un átomo de carbono trivalente y con carga negativa. Estos tienen una geometría tetrahedral, con un par de electrones ocupando uno de los orbitales sp3:
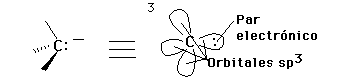
Se sabe que hay grupos que pueden donar o pueden atraer electrones a través de un enlace sigma. Esto se conoce como efecto inductivo. Por ejemplo, los grupos alquilo (R) donan electrones por efectos inductivos.
En el caso de los carbaniones, a mayor número de grupos alquilo mayor la inestabilidad del intermediario. Esto se debe a que el efecto inductivo intensifica la carga negativa, desestabilizando el sistema. De aquí que la estabilidad relativa de los carbaniones sigue la siguiente secuencia:
metílico > primario > secundario > terciario

¿Qué es un carbocatión?
Un carbocatión es un carbono trivalente con una carga positiva. Contrario al carbanión, que es tetrahedral, el carbocatión es trigonal planar y su hibridación es sp2. El ángulo de enlace es de 120°.

Los carbocationes tienen deficiencia de electrones, por lo que se clasifican como electrófilos. Por el efecto inductivo de donación de electrones, los grupos alquilo dispersan la carga positiva del carbono, estabilizando el sistema.
Otro efecto que estabiliza a los carbocationes es el de resonancia, específicamente la hiperconjugación: solapamiento de orbitales sp3 con el orbital p de carbono positivo. A mayor número de grupos alquilo, mayor la hiperconjugación y mayor la estabilidad del carbocatión.

Como los carbocationes con mayor número de grupos alquilo son los más estables, el orden de estabilidad sigue la siguiente secuencia:
terciario > primario > secundario > metílico

Una de las caracteristicas más importantes de los carbocationes es su tendencia a rearreglarse a un carbocatión más estable, ya sea por un desplazamiento de hidruro o por el desplazamiento de alquilo. El rearreglo es siempre de un carbocatión menos estable a uno más estable:

¿Qué es un carbeno?
Un carbeno es un compuesto que contiene un carbono divalente con sólo seis electrones de valencia: cuatro de éstos en dos enlaces covalentes y dos electrones de no-enlace. El miembro más simple de estos compuestos es metileno, :CH2

Se conocen carbenos substituídos del tipo RHC: y R2C: , en los que el substituyente R va desde grupos alquilos y arilos hasta halógenos y grupos acilo.
El carbono tiene cuatro orbitales atómicos disponibles capaces de contener hasta ocho electrones de valencia. Como el carbeno sólo utiliza dos orbitales moleculares de enlace, los dos electrones de no-enlace se acomodan en los dos orbitales atómicos que sobran.
Estos dos electrones pueden acomodarse en estos orbitales de dos maneras:
(1) ocupando ambos un mismo orbital, o
(2) ocupando cada uno un orbital diferente.
Si los dos electrones de no-enlace ocupan el mismo orbital, éstos deben tener giros opuestos, es decir, deben estar pareados. En este caso, nos referimos al carbeno singulete. La hibridación en este carbeno es sp2 , y los dos electrones de no- enlace ocupan uno de estos orbitales (par solitario). El orbital "p" que no hibridizó permanece vacante:

La estructura del carbeno singulete es análoga a la estructura de un carbocatión.
Cuando los dos electrones de no-enlace ocupan orbitales diferentes, entonces nos referimos al carbeno triplete, en el que la hibridación del carbono central es sp y los electrones de no enlace se encuentran en los orbitales "p" sin hibridizar. El giro de ambos es paralelo:

El carbeno triplete tiene menos energía que el carbeno singulete. Por poseer un electrón en cada orbital "p" se considera como un diradical.
¿Qué es un radical?
Se define un radical (o radical libre) como aquella molécula o átomo que contiene, al menos, un electrón sin parear.
La estructura de un radical simple es similar a la de un carbocatión: plana o casi plana, con el carbono central hibridizando sp2. El electrón impar está localizado en el orbital "p" que quedó sin hibridizar:

Al igual que los carbocationes, los radicales libres están deficientes de electrones, por lo que son electrófilos. Por el efecto inductivo de donación de electrones de los grupos alquilo, la estabilidad de los radicales libres sigue el mismo orden que los carbocationes: a mayor número de grupos alquilo, mayor la estabilidad del radical libre. Asi, el orden de estabilidad relativa sigue la secuencia:
terciario > secundario > primario > metilo

Contrario a los carbocationes, es muy raro el rearreglo de un radical menos estable a uno de mayor estabilidad.
¿Qué significa la selectividad de un intermediario?
Se dice que un intermediario es selectivo si éste demuestra un amplio recorrido de velocidades de reacción frente a diferentes moleculas. Esta selectividad usualmente está asociada a un intermediario relativamente estable: el tiempo de existencia del intermediario es lo suficientemente amplio como para que éste pueda escoger, cuidadosamente, entre las alternativas disponibles. Este tipo de intermediario se forma con relativa lentitud.
Un intermediario menos estable reacciona más indiscriminadamente con las moléculas disponibles, de aquí que sea menos selectivo y más reactivo. La formación de este intermediario es relativamente rápida.