Clique aqui para fechar esta janela Voltar a página anterior
| MUDANÇA DE FASE |
INTRODUÇÃO
Diariamente convivemos com substâncias sólidas, líquidas e gasosas. Sob determinadas condições, é possível mudar a fase de uma substância. É do nosso conhecimento, por exemplo, que a água líquida pode ser transformada em água sólida ou em vapor de água.
O ponto fundamental nesse estudo é o fato de a fase de uma substância ser determinada pela temperatura ( T ) e pela pressão ( p ) a que ela é submetida. Assim, dependendo desse par de valores ( T e p ), a substância pode estar em qualquer uma das fases (sólida, líquida ou gasosa), ou até mesmo em uma situação que corresponda ao equilíbrio entre duas ou entre três fases.
MUDANÇA DE FASE
A mudança de fase é um fenômeno térmico que uma substância sofre ao alterar seu estado físico.
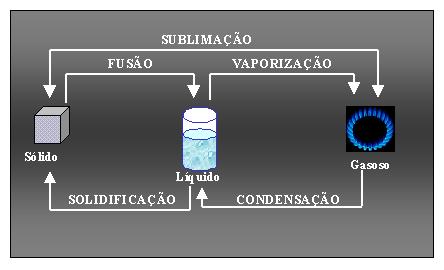 |
ATENÇÃO: NÃO CONFUNDIR EVAPORAÇÃO COM EBULIÇÃO
EVAPORAÇÃO
É o tipo de vaporização lenta, que ocorre apenas junto à superfície livre do líquido. Esse fenômeno não requer condições físicas determinadas para ocorrer. Em outras palavras, não há uma temperatura determinada para um líquido evaporar. A água do tanque, por exemplo, evapora a 5o C, a 20o C, a 60o C , etc.
EBULIÇÃO OU VAPORIZAÇÃO
É a vaporização intensa e turbulenta que ocorre ao longo de toda a massa líquida, com formação de bolhas de vapor junto às superfícies aquecidas. Essa bolhas aumentam de volume à medida que se elevam no líquido, em virtude da redução da pressão. Ao contrário da evaporação, a ebulição só acontece quando é atingida uma certa temperatura, que depende da pressão exercida sobre o líquido pelo ambiente.
CONCEITOS BÁSICOS
Ponto de fusão é a temperatura na qual a substância muda da fase sólida para a fase líquida.
Ponto de vaporização é a temperatura na qual a substância muda da fase líquida para a fase gasosa.
|
substância |
Ponto de fusão ( o C ) |
Ponto de vaporização ( o C ) |
|
mercúrio |
-39 |
357 |
|
nitrogênio |
-210 |
-196 |
|
álcool |
-115 |
78 |
|
enxofre |
119 |
420 |
|
gelo |
0 |
----- |
|
prata |
961 |
----- |
|
água |
----- |
100 |
Ponto de condensação é a temperatura na qual a substância muda da fase gasosa para a fase líquida.
Ponto de solidificação é a temperatura na qual a substância muda da fase líquida para a fase sólida.
PONTO DE VAPORIZAÇÃO EM ALGUNS LUGARES
Em alguns lugares, o ponto de vaporização pode variar dependendo da altitude local.
Maceió, Recife e Rio de Janeiro 100o C
São Paulo 98o C
Brasília 96o C
Quito 90o C
La Paz 87o C
Alto do Monte Everest 75o C
CALOR LATENTE
É a quantidade de calor que uma substância recebe para mudar de fase quando a mesma se encontra no ponto de fusão, ou no ponto de vaporização, ou no ponto de solidificação, etc.
|
Substância |
Calor latente de fusão (cal / g) |
Calor latente de vaporização ( cal /g ) |
|
mercúrio |
2,8 |
65 |
|
nitrogênio |
6,09 |
48 |
|
álcool |
2,5 |
204 |
|
enxofre |
13,2 |
62 |
|
gelo |
80 |
----- |
|
oxigênio |
3,3 |
51 |
|
água |
----- |
540 |
FÓRMULA DO CALOR LATENTE
|
Q = m . L Q .... Quantidade de calor necessária à mudança de fase quando a substância está no ponto de mudança. m .... massa da substância. L .... calor latente de mudança de fase da substância. |
FÓRMULA DO CALOR SENSÍVEL
|
Q = m . c . Dt Q .... Quantidade de calor necessária a uma variação de temperatura. m .... massa da substância. Dt .... variação de temperatura. |