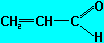1. O carbono é tetravalente (faz quatro ligaçőes simples);
2. As ligaçőes do carbono săo equivalentes e coplanares (săo iguais e ocupam o mesmo plano do espaço);
 3. Átomos de carbono podem ligar entre si formando cadeias.
3. Átomos de carbono podem ligar entre si formando cadeias.Como dito anteriormente, os compostos orgânicos sempre contém carbono, por isso é muito importante o conhecermos melhor.
Durante o século XIX o problema năo era saber a composiçăo dos compostos, mas saber como os átomos se uniam. Surgiu entăo o postulado de Kekulé, que dizia:
1. O carbono é tetravalente (faz quatro ligaçőes simples);
2. As ligaçőes do carbono săo equivalentes e coplanares (săo iguais e ocupam o mesmo plano do espaço);
 3. Átomos de carbono podem ligar entre si formando cadeias.
3. Átomos de carbono podem ligar entre si formando cadeias.
A teoria de Kekulé dizia que a estrutura do carbono era plana, mas com o avanço da química orgânica percebeu-se que essa estrutura năo explicava algumas das observaçőes verificadas em algumas das novas substâncias.
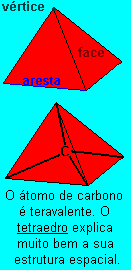
Em 1874, Van't Hoff e Le Bel criaram um novo modelo para a estrutura espacial das ligaçőes do carbono. Este novo modelo propunha uma estrutura em forma de tetraedros regulares, onde o núcleo do átomo de carbono ocuparia posiçăo central, e suas ligaçőes nos vértices.
Assim, se houvesse uma ligaçăo simples os tetraedros se uniriam pelos vértices. Em uma ligaçăo dupla os tetraedros se ligariam por dois vértices (uma aresta) e em uma ligaçăo tripla eles se ligariam por tręs vértices (uma face). Esse modelo explica muito bem por que o carbono năo faz uma ligaçăo quádrupla: por falta de espaço.
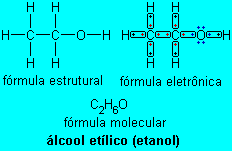
Quando esse modelo foi criado ainda năo se conheciam os elétrons, sendo que, depois de criado o atual modelo atômico de Rutherford-Böhr, Lewis propôs que os átomos se ligassem através de pares eletrônicos na camada de valęncia. Tal representeçăo é conhecida por Fórmula Eletrônica de Lewis:
Após criado esse modelo houve algumas mudanças na ligaçăo covalente e foi desenvolvida a teoria da hibridaçăo.
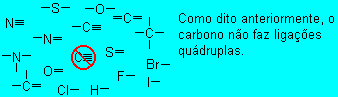
Năo é só o carbono que participa dos compostos orgânicos. Quase sempre existe existe também hidrogęnio (monovalente), oxigęnio (bivalente) e outros. Os mais frequentes săo: enxofre (bivalente), nitrogęnio (trivalente) e halogęnios (monovalentes).
É muito importante conhecer também as cadeias formadas por átomos de carbono. Veja um exemplo:

Veja que um átomo de oxigęnio está em destaque. Outros átomos também podem estar na cadeia carbônica, com a condiçăo que esteja entre dois átomos de carbono. Tal átomo é denominado de heteroátomo.
Cadeia carbônica é a estrutura formada por todos os átomos de carbono e heteroátomos de uma molécula orgânica |
Pode-se representar os compostos orgânicos de uma forma mais simplificada:

Classificaçăo das cadeias carbônicas
As cadeias săo classificadas da seguinte maneira:

A glicerina tem cadeia carbonica com extemos livres. É uma cadeia carbônica aberta (acíclica ou alifática). já o ciclobuteno năo apresente extremos livres: Tem cadeia carbônica fechada (ou cíclica).
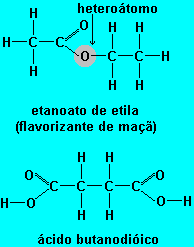
O etanoato de etila tem cadeia carbônica heterogęnea pois existe um átomo de oxigęnio entre dois carbonos (heteroátomo).
Enquanto o ácido butanodióico tem cadeia carbônica homogęnea, pois há apenas átomos de carbono (lembrando que os quatro átomos de oxigęnio dessa molécula năo săo heteroátomos, pois năo estăo entre dois carbonos).
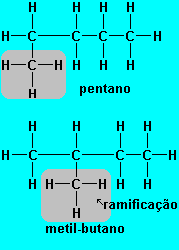
A molécula de pentano é normal (ou năo-ramificada), pois, em cadeias abertas, tem apenas dois extremos. A parte destacada năo é ramificaçăo, pois năo existe ramificaçăo no final da cadeia.
O metil-butano no entanto tem cadeia carbônica ramificada, pois apresenta mais de dois extremos.
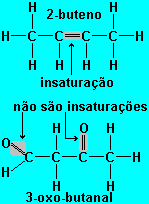
Se existir uma ou mais ligaçőes duplas ou triplas entre carbonos a cadeia será classificada como insaturada, sendo q esta dupla será chamada de insaturaçăo.
Insaturaçăo é uma ligaçăo dupla ou tripla entre átomos de carbono. |
Portanto o 2-buteno tem cadeia carbônica insaturada
Já o 3-oxo-butanal tem cadeia saturada. Vale lembrar que as duplas ligaçőes destacadas năo săo insaturaçőes, pois năo estăo entre carbonos.
Também pode-se classificar as cadeias carbônicas fechadas em aromáticas ou năo-aromática. Uma cadeia aromática contém anel benzęnico.
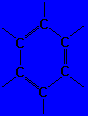 Anel benzęnico é uma estrutura cíclica que contém seis átomos de carbono com duplas e triplas intercaladas. |
Devido o efeito da ressonância a representaçăo mais usada para representar o anel benzęnico é: 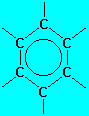 |
Entăo podemos classificar as cadeias carbônicas a seguir como:
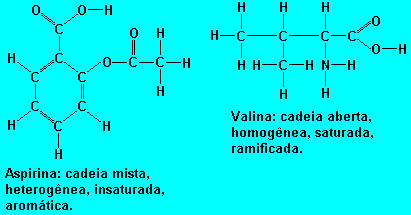
Para facilitar a comunicaçăo entre os químicos a IUPAC(Uniăo Internacional da Química Pura e Aplicada) criou regras que facilitam a nomenclatura das substâncias.
| Número de carbonos | Prefixo |
| 1 | met |
| 2 | et |
| 3 | prop |
| 4 | but |
| 5 | pent |
| 6 | hex |
| 7 | hept |
| 8 | oct |
| 9 | non |
| 10 | dec |
| 11 | undec |
| 12 | dodec |
| Tipos de ligaçőes | Intermediário |
| apenas simples | an |
| uma dupla | en |
| duas duplas | dien |
| uma tripla | in |
| duas triplas | diin |
| uma dupla e uma tripla | enin |
| Funçăo | Sufixo |
| hidrocarboneto | o |
| álcool | ol |
| aldeído | al |
| cetona | ona |
| ácido carboxílico | óico |
Essas tabelas săo necessárias para formular a nomenclatura dos compostos orgânicos, mas muitas vezes usam-se outros artifícios. Por exemplo: a funçăo ester năo está na terceira tabela, pois para sua nomencletura é necessário outras técnicas.
Vamos a um exemplo: vocę ainda năo aprendeu, mas o seguinte composto é um aldeído. Seu nome seria: propenal.