Prefacio
1. Mecánica
2. Propiedades de los Fluidos
3. Gases
4. Fenómenos Térmicos
5. Sonido y Luz
6. Varias
7. Apéndice

212. Una vela dentro de un tarro tapado.
Ofrecemos la descripción de un experimento para comprobar la influencia de la presión atmosférica, que fue publicada en su tiempo en una revista para escolares:
«Un cabo de vela encendido se fija al fondo de un tarro de vidrio; después de que permanezca encendido algún tiempo, la vasija se tapa poniendo un aro de goma húmedo entre sus bordes y la tapa. Al poco rato la llama empieza a extinguirse y se apaga. Si usted trata de destapar el tarro, podrá lograrlo aplicando un esfuerzo bastante considerable.
Es fácil comprender la causa de este fenómeno. La llama consume oxígeno, cuya reserva está limitada en este tarro herméticamente tapado. Cuando el oxígeno se agota, la llama se apaga. El resto de aire que ocupa un volumen mayor, se rarifica y ejerce una presión menor. La tapa queda apretada fuertemente a los bordes del recipiente por el exceso de presión exterior.»
żEs correcta esta explicación?
 |
| Un cabo de vela colocado en un tarro de cristal |
La explicación del experimento es incorrecta. En lugar del oxígeno consumido mientras la vela estaba ardiendo se ha formado bióxido de carbono: en la proporción de una molécula de éste por cada dos moléculas de aquel. Un número igual de moléculas siempre ocupa un mismo volumen si la presión no varía (ley de Avogadro). Por consiguiente, el consumo de oxígeno de por sí no puede alterar la presión del gas contenido en el tarro.
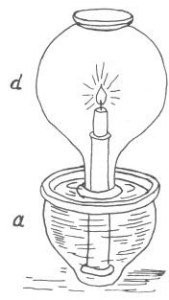 |
| El experimento con una vela encendida descrito por Filón |
La causa real del fenómeno en cuestión es distinta, no es de carácter químico, sino físico. Naturalmente, dentro del recipiente el aire se enrarece durante la combustión, pero no a consecuencia del consumo de oxígeno, sino debido al calentamiento. Parte del gas dilatado sale del tarro hasta que se igualen la presión del aire exterior frío y del caliente contenido en el recipiente. Cuando la vela se apaga por falta de oxígeno, el aire dentro del recipiente se enfría, su presión disminuye, y el exceso de presión atmosférica aprieta la tapa a los bordes de la vasija.
Es harto conocida una modificación de este experimento: un vaso en el cual previamente se coloca un trozo de papel ardiendo, se pone boca abajo en un plato con agua y esta última entra en el vaso. Muchas veces este fenómeno se atribuye al consumo del aire: incluso se llega a afirmar a veces que el agua «siempre sube hasta 1/5 parte de la altura del vaso, con arreglo a la proporción del oxígeno presente en el aire», aunque nunca se ha observado semejante constancia.
Este equívoco se ha generalizado mucho. Por ejemplo, en su obra Ciencias naturales vistas en su desarrollo e interrelación, aparecida a principios del siglo XX, F. Dannemann decía lo siguiente:
«En la figura aparece la vela de Filón que succiona líquido. El recipiente a contiene agua. El recipiente d está invertido de modo que su boca se hallaba bajo el agua y dentro de él se encuentra una vela encendida. "El agua, dice Filón, enseguida empieza a subir. Esto sucede porque el fuego desplaza aire del recipiente d. El volumen del agua que entra en el segundo recipiente equivale al del aire desplazado."
El sabio no se dio cuenta de que cada vez se desplaza una misma cantidad de aire. En este caso se trata de una de las experiencias realizadas por Scheele y otros experimentadores para demostrar el hecho de que el aire consta de dos gases diferentes.»
Según vemos, la explicación sugerida por el físico de la Antigüedad, en principio, muy correcta, se da por incorrecta en el fragmento que acabamos de citar; más aún, lo que se afirma es del todo incorrecto desde el punto teórico y práctico.
|
|
|
|