Техническое обеспечение аквакультуры
подразумевает применение устройств и технологий
обеспечивающих оптимальный режим содержания
рыбы в искусственных условиях и имитирующих
процессы происходящие в натуральных биотопах.
- Обеззараживание
воды.
- Биологическая
очистка воды.
- Ионобмен.
- Адсорбция.
- Аэрация
- Температурный
режим.
- Аквасистемы и
рыбоводные емкости.
- Инкубационные
системы.
Обеззараживание воды
Озонирование воды
Физико-химические свойства и
получение озона. Озон - газ
бледно-фиолетового цвета. при температуре -119°С
озон превращается в нестойкую жидкость
темно-синего цвета. Озон тяжелее воздуха.
Коэффициент растворимости в воде при
температуре 0° - 0,49, при температуре 20° - 0,29.
Обеззараживающее действие озона основано на
высокой окислительной способности,
обусловленной легкостью отдачи им активного
атома кислорода (О3=O2+O). Озон окисляет
все металлы, кроме золота, превращая их в оксиды.
В водном растворе озон диссоциирует быстрее, чем
в воздухе; очень быстро диссоциирует в
слабощелочных растворах. В кислотных растворах
озон проявляет большую стойкость. В чистом сухом
воздухе он разлагается очень медленно.
Озон получают пропусканием воздуха или
кислорода через электрический разряд высокого
напряжения. Для организации процесса получения
озона устраивают разрядную камеру. В камере
электрический разряд проходит через слой
диэлектрика, воздуха и снова диэлектрика.
Непосредственно в слое воздуха разрядной камеры
и происходит образование озона. От величины
зазора между слоями диэлектрика зависит
производительность озонатора.
Бактерицидное действие озона. Высеваемые
после озонирования воды штаммы (ранее
вирулентных микробов) с измененными
морфологическими, биохимическими и
культуральными свойствами могут утрачивать
вирулентность или снижать ее. С повышением
температуры воды необходимо также увеличивать
дозу озона для получения одинакового эффекта
обеззараживания. С повышением температуры воды
повышается количество не использованного озона.
Увеличение рН более 7,1 сопровождается
значительным возрастанием бактерицидной дозы
брутто-озона, в то время как нетто-озон не
изменяется. С повышением значения рН уменьшается
коэффициент использования водой.
Мутность до 5 мг/л на обеззараживание воды озоном
оказывает незначительное влияние; прибольшей
мутности бактерицидное действие озона
значительно ухудшается. Для получения
бактирицидного эффекта при мутности 5 мг/л
необходимо 2 мг/л озона, при 10 мг/л - 3,6 мг/л, при 50
мг/л - 6,4 мг/л и, наконец при 100 мг/л - 9,6 мг/л озона.
На обеззараживающее действие озона влияет
цветность воды, обусловленная легко
окисляющимися органическими веществами из
группы гумусовых (гуминовых) кислот. Увеличение
цветности в два раза приводит к увеличению
бактерицидной дозы озона-нетто в 2,9 - 1,6 раза.
Эффективность обеззараживания воды при разной
исходной цветности показали, что в начале
озонирования количество бактерий снижается
незначительно, так как озон расходуется на
окисление гуминовой кислоты, что приводит к
значительному снижению цветности. Вследствие
окисления гуминовых кислот в воде все больше
накапливаются стойкие к окислению слвбо
окрашенные или бесцветные соединения. В конце
озонирования поданый в воду озон еще меньше
расходуется на окисление органических веществ и
оказывает бактерицидное действие, вследствие
чего кривая оставшихся в воде жизнеспособных
бактерий круто идет вниз. Полное обеззараживание
воды наблюдается при снижении цветности до 8,6 -
10,4°.
Озон разрушает также спорвые бактерии, на
которые он действует примено в 300 - 600 раз сильнее,
чем хлор.
Действие озона на вирусы. Озон оказывает
более активное действие на вирусы по сравнению с
хлором. Это объясняется тем, что озон оказывает
влияние на окислительно-восстановительную
систему и на протоплазму клетки, а хлор разрушает
только ферменты микробной клетки. Как известно,
вирусы не иеют ферментных систем. Озонирование
воды является эффективным методом
обеззараживания в отношении энтеровирусов.
Обезвреживание в воде фенолов.
Озонирование фенолсодержащей воды разрушает
фенол до оксалатов и бикарбонатов. Окисление
фенолов озоном протекает в несколько стадий, в
процессе которых образуются как продукты
глубокой деструкции, так и продукты начального
окисления хиноидной структуры. Продукты
озонирования фенола и гидрохинона не только не
токсичны, но и практически некумулятивны.
Ультрафиолетовое излучение
|
Обеззараживание УФ-излучением
производят при условии, что вода обладает малой
цветностью и не содержит коллоидных и взвешенных
веществ, поглощающих и рассеивающих
ультрафиолетовые лучи. Эффект обеззараживания
основан на прямом губительном воздействии
ультрафиолетовых лучей ( в спектре с длиной волны
200 - 300 нм. ) на белковые коллоиды и ферменты
протоплазмы микробных клеток. УФ-излучение может
воздействовать не только на обычные бактерии, но
и на споровые организмы и вирусы.
Ультразвук
|
Ультразвуковые волны обладают
бактерицидным действием. Это действие
возрастает с увеличением интенсивности
ультразвукового поля и продолжительности
воздействия на воду.
Импульсный электрический разряд
|
Импульсный электрический разряд
сопровождается мощными гидравлическими
процессами с образованием ударных вод и явлений
кавитации, интенсивными ульразвуковыми
колебаниями и возникновением импульсных
магнитных и электрических полей.
Для обеззараживания воды необходимо создать
плотность энергии 15 Дж/мл.
** Практическая
часть
Биологическая очистка воды
Цикл азота в водной среде
|
В процессе эксплуатации рыбоводной
установки в нее неизбежно поступает азот. Прежде
всего азот выделяется животными ( в в форме
аммиака, мочевины, аминокислот и т.д. ). Кроме того,
азотсодержащие вещества выделяются в процессе
бактериального разложения растений, животных и
остаткаов корма. Азотсодержащие отходы
постепенно превращаются в аммиак, который путем
нитрификации переходит в нитраты через нитриты NO2-.
Этот процесс осуществляется аэробными
бактериями. Бактерии Nitrosomonas обеспечивают
превращение аммиака в нитриты, а Nitrobacter - нитритов
в нитраты. В замкнутых циркуляционных системах,
где отсутствуют фотосинтезирующие организмы,
концентрация нитратов может оказаться
черезмерно высокой. Для вывода последних из
оборота возможно прибегнуть к использованию
анаэробных процессов или частичной подмене воды.
В анаэробных процессах учавствуют бактерии
Pseudomonas, Achrobacter, Bacillus и др. Для своего дыхания эти
бактерии используют кислород содержащийся
нитратах и тем самым освобохдают азот, который
выходит из системы в форме газа. Для инициации
процесса денитрификации, концентрация кислорода
должна быть не более 2 мг/л., если же кислорода
будет больше указанной границы, бактерии начнут
брать его не из нитратов, а из воды.
Принцип биологической очистки воды
|
Все выше описанные процессы
могут происходить в аквариуме сами собой, как это
происходит в природных водоемах, но
самоочистительная мощность воды пригодной для
жизни рыб не велика - 0,03 мгр02/л.час. Поэтому
обеспечить полноценные условия существования
для рыб, не устраивая специальной очистительной
системы, можно лишь предоставив им объем воды,
который будет способен перерабатывать в
нетоксичные соединения отходы
жизнедеятельности аквариума.
Активизировать очистку воды от соединений азота,
можно поселив в аквариуме колонию
микроорганизмов способных поглощать
поступающие в воду примеси. Для этого нужно
создать микроорганизмам благоприятные условия.
Поставленная задача решается при устройстве
биофильтров или аэротенков.
Биофильтр - это система состоящая из
субстрата для закрепления колонии
микроорганизмов. Для организации биофильтра
необходимо обеспечить транспорт питательных
веществ (азотных соединений растворенных в воде)
к колонии микроорганизмов и поступление
кислорода в тело субстратной загрузки.
Попав в биофильтр, грязная вода вступает в
контакт с биопленкой, в результате чего
происходит первая фаза очистки - адсорбция
органики на биопленке. Если вода проходит через
субстрат биофильтра непрерывно, то процесс
адсорбции и следующий за ним этап - окисление,
идут постоянно и параллельно друг другу. При
циклической подаче воды эти процессы
разделяются на два последовательных. Первый
будет идти интенсивно при фазе орошения, а второй
при фазе вентиляции.
Для обработки поступивших загрязнений требуется
определенное время, которое будет зависеть от
количества подаваемого кислорода. Если кислород
поступает в биофильтр с загрязненной водой, то
окисление адсорбированных соединений
происходит за 1 -2 часа. При обеспечении дыхания
биофильтра кислородом из воздуха, на окисление
адсорбированных веществ требуется 12 минут.
Следовательно увеличить производитетельность
биофильтра можно не только увеличивая его
размеры, но и увеличивая доступ кислорода к
биопленке.
Объем субстрата помещаемого в тело биофильтра
зависит от количества рыб создающих нагрузку на
рыбоводную систему. Поперечное сечение
фильтрующего слоя определяется гидравлической
нагрузкой на фильтрующий блок, она не должна
превышать 20 - 30 л/дм2час. Толщина
фильтрующего слоя является производной скорости
воды и содержания в ней кислорода. Чем больше
скорость воды проходящей через биофильтр и выше
концентрация растворенного кислорода, тем более
толстый слой фильтрующего материала находится в
условиях аэробного дыхания.
Аэротенк - это система состоящая из
емкости и блока барботажа воды. Чистящим агентом
здесь является активный ил, который циркулирует
по емкости в заданном режиме. Сама емкость
устраивается таким образом, чтобы весь объем
поступающей в нее воды эффективно перемешевался
с активным илом, не образовывал застойных зон и
хорошо обогащался кислородом. Попав в такие
условия анаэробные бактерии гибнут, а аэробные
включаются в состав активного ила. для создания
такого режима необходимо обеспечить постоянную
аэрацию очищаемой воды и стабильное поступление
органического вещества. Последнее условие
необходимо для того, чтобы не создавались
экстремальные ситуации (например недостаток или
избыток питательных веществ), так как это
неизбежно отразится на биоценозе активного ила.
После того как активный ил переработает
поступившие к нему питательные вещества, он
должен быть отделен от очищенной воды и
возвращен к началу своего пути, где он снова
вуступит в реакцию с органическими веществами.
Для отделения ила от чищенной воды устраивается
сепаратор или отстойник, где ил оседает на дно и
перекачивается в аэротенк.
Активный ил представляет собой биоценоз
микроорганизмов минерализаторов, способных
сорбировать своей поверхностью и окислять в
присутствии кислорода органические вещества.
Образование активного ила происходит по причине
того, что все виды бактерий при определенных
условиях могут образовывать скопления благодаря
склеиванию их капсул (зооглейные скопления здесь
не являются причиной). Хлопья активного ила имеют
размер 0,1 - 0,5 мм. Примечательной особенностью
активного ила является очень развитая
поверхность, на 1 гр. ила приходится 1,0х1012
бактерий с суммарной поверхностью 1200 м2.
** Практическая
часть
Ионообмен.
В практике аквариумной водоподготовки
важное место занимает возможность корректировки
ионного состава воды оборачиваемой в
аквасистеме. В рыбоводстве с этой целью
применяются иониты.
Иониты бывают органические и
неорганические. Кроме того они могут иметь
натуральную или искусственную природу. К
неорганическим природным ионитам относятся
цеолиты, глинистые минералы, полевые шпаты,
различные слюды и др. Катионообменные свойства
их обусловлены содержанием алюмосиликатов. К
неорганическим синтетическим ионитам относятся
силикагели,пермутиты, гидроксид алюминия,
гидроксид хрома и др. Органические природные
иониты - это гуминовые кислоты почв и углей. они
проявляют слабокислые свойства. Для усиления их
кислотных свойств и обменной емкости угли
измельчают и сульфируют в избытке олеума.
Сульфоугли являются дешевыми полиэлектролитами,
содержащими сильно и слабокислотные группы. К
недостаткам таких ионитов следует отнести их
малую химическую стойкость и механическую
прочность зерен, а также небольшую обменную
ёмкость, особенно в нейтральных средах. К
синтетическим органическим ионитам относятся
ионообменные смолы.
Наиболее перспективно и целесообразно
на сегодняшний день использование для
водоподготовки полимерных ионообменных смол.
Ионобменные смолы можно разделить на
четыре группы: сильнокислые катионы, слабокислые
катионы, сильноосновные анионы и слабоосновные
анионы. Эта классификация основана на способе
изготовления, а также на свойствах материала.
Воду пропущенную предварительно через катионит
принято называть катионированной, через анионит
- анионированной. Катиониты в качестве
противоионов могут содержать как ионы водорода
так и ионы металлов, т. е. находиться в солевой
форме. точно также и аниониты могут находиться в
солевой форме.
Иониты в контакте с водой не
растворяются, но поглощают некоторое количество
воды и набухают, являясь гелями с ограниченной
набухаемостью. Набухание влияет на скорость и
полноту обмена ионов, а также на селективность
ионита.
Установлены ряды ионов по энергии их
вытеснения из сильно- и слабо кислотных катионов.
Например, сильнокислотного сульфокатиона КУ-2
получен следующий ряд:
H+ - Na + - NH4+ - Mg2+
- Zn2+ - Co2+ - Cu2+ - Cd2+ - Ni2+
- Ca2+ - Sr2+ - Pb2+ - Ba2+
Иониты выпускают в виде порошка
(размер частиц 0,04 - 0,07 мм), зерен (0,3 - 2,0),
волокнистого материала, листов и плиток. В
маркировке смол для катионитов употребляют
букву К, для обозначения анионитов - А. В таблице
приведенной ниже даны ряд отечественных ионитов
и их зарубежных аналогов:
| КУ-2-8 |
Амберлит IR-120, дауэкс-50, диайон, SK-1A,
зеролит 225, имак С-12, вофатит KRS-200, варион KS,
дуолайт С-20, алласьон CS, кастель С-300Р, катекс-5 |
| КУ-23 |
Леватит SP-120, кастель С-300Р, амберлит 15А,
варион KSM |
| КБ-2, КБ-2-4 |
Варион KSM, вофатит СР, дуолайт СС-3, йонайк
С-270, пермутит Н-70, пермутит С |
| КБ-2-7П, КБ-2-10П |
Варион KSM, дуолайт С-464, имак Z-5 |
| КБ-4, КБ-4П-2 |
Амберлит IRA-50, варион СР, зеролит 226,
цеокарб 226 |
| АВ-17-8 |
Амберлит IRA-400, дауэкс-1, зеролит FF, дуолит
A-101D, кастель А-500, диайон SA-10A, вофатит SBW, леватит
М-500,варион АТ-660 |
| АВ-29-12П |
Дуолайт А-162, варион AMD, диайон РА-404,
леватит МР-600, амберлит А-29, амберлит IRA-910, релит 2AS |
| АН-22-8 |
Варион AED |
| КУ-1 |
Амберлит IRA-100, йонайк С-200, вофатит К |
| ЭДЭ-10П |
Дуолайт А-30, кастель А-100, вофатит L-150,
вофатит L-160, вофатит L-165 |
| АН-2ФН |
Амберлит IR-4B |
Из характеристик которыми
обладают иониты, наиболее важной в аспекте
аквариумистики является полная обменная емкость
измеряемая в г-экв/м3 - количество ионов
поглощенных единицей объема ионита.
| КУ-2 |
1300-1800 |
| КУ-2-8 |
1800 |
| КУ-1 |
1400 |
| КБ-4 |
4200 |
| АВ-17-8 |
1300-1500 |
| ЭДЭ-10П |
1300-1500 |
| АН-2Ф |
3700 |
| АН-22 |
4050-4550 |
Работа ионита заканчивается в
момент наступления "проскока", когда в
фильтрате обнаруживаются поглощаемые ионы. В
эксплуатации такое состояние фильтрующей среды
как рабочая емкость. Естественно величина
"проскока" различна при Н-катионировании
Na-катионировании
| Марка иоонита |
Н-катионирование |
Na-катионирование |
| Сульфоуголь СМ-1 |
250 |
400 |
| КУ-2 |
800 |
800 |
| Вофатит Р |
300 |
300 |
Как правило потребности аквариумного хозяйства
относительно ионобменных материалов лежат в
плоскости проблем понижения жесткости
потребляемой воды. Как известно жесткость воды
обусловлена содержанием ионов кальция и магния.
Извлечение ионов металлов из водной среды
обеспечивается катионированием, что позволяет
исключить из процесса ионообмена стадию
обработки анионитом. Проведение
Н-катионирования влечет за собой значительное
понижение рН, это качество можно использовать
при необходимости коррекции кислотности воды.
Na-катионирование сдвигов по показателю рН за
собой не влечет.
Отработанныые иониты возможно регенерировать.
В промышленной практике
водоподготовки существуют различные схемы
регенерации отработанных ионитов. Для
аквариумного хозяйства рядом положений можно
пренебречь, ввиду относительной малости обьемов
обрабатываемой воды. Важно соблюсти саму химию
восстановления ионитов и обеспечить
законченность реакций.
Катиониты регенерируют 2-8%-ми растворами кислот.
При этом они переходят в Н-форму. Регенерационные
растворы - элюаты содержат катионы. Для
регенерации одного объема смолы требуется пять
объемов элюата. Реакцию можно проводить либо
посредством пропускания элюата через массив
ионита, либо замачиванием и перемешиванием смолы
с элюатом. Процесс регенерации может длиться до 40
минут. Затем после взрыхления и промывки
катиониты заряжаются, например в Na-форму, путем
пропускания через них раствора поваренной соли.
Тогда Н-функциональные группы, получающиеся при
регенерации катионита кислотой, заменяются на
Na-группу, а используемый для зарядки раствор
поваренной соли подкисляется до соляной кислоты.
На степень регенерации влияет тип ионита,
природа, концентрация и расход регенерирующего
вещества, температура, время контакта и расход
реагентов. После завершения регенерации
ибязательно промывка ионита от продуктов
регенерации и остатков не прореагировавшего
раствора. На отывание ионита требуется десять
объемов дистиллированой воды. После окончания
отмывки ионит может сразу включаться в работу
или резервируются.
Собственно запуск новых ионитов в
работу заключается в замачивании и формировании
активной ионной группы. При замачивании иониты
набухают и размер их микропор возрастает 0,5-1,0 нм.
до 4 нм., объем смолы увеличивается
соответственно в 1,5-3 раза. Набухание
прекращается после того как разность
осмотических давлений до и после обмена
уравновесится упругими силами сжатия и
растяжения ионита. Относительно ионной группы,
нужно знать, что свежие иониты Н-активны.
** Практическая
часть
Адсорбция.
Адсорбция -
поглощение поверхностью твердого тела
какого-либо компонента из газа или жидкости. При
очистке воды адсорбция происходит либо на
поверхности раздела между жидкостью и твердым
телом, например между активированным углем и
водой, либо на поверхности раздела между
жидкостью и газом, например между воздухом и
водой при пенном фракционировании.
Посредством адсорбции
возможно извлекать из воды: фенолы,
хлорорганические пестициды, частично аммиак и
азотистые соединения, мочевину, гуминовые
кислоты, свободный хлор, красители и
лекарственные препараты.
В условиях пресноводного
аквариума наибольшее распространение имеет
адсорбция посредством активированного угля.
Адсорбция на активированном угле - это процесс
протекающий в два или три этапа в зависимости от
участка, где происходит адсорбция.
На первом этапе, называемом пленочной диффузией,
происходит перенос растворенного вещества
сквозь пленку на поверхности активированного
угля. Втрой этап - поровая диффузия - характерна
диффузией адсорбата в порах или трещинах
адсорбента. Адсорбат который адсорбируется на
внешней стороне активированного угля, эту стадию
минует. Третий этап - фактическая адсорбция
адсорбата на поверхности активированного угля.
Эффективность процесса зависит от многих
переменных. Большая часть этих параметров не
контролируется в условиях любительского
аквариумного хозяйства. Тем не менее некоторые
соотношения установить можно.
Площадь поверхности. С
уменьшением размера частиц угля площадь
поверхности активированного угля увеличивается,
соответственно увеличивается и масштаб
адсорбции. Однако, мелкие частицы в неподвижных
слоях быстро приводят к закупорке пор твердыми
веществами, а также потере напора.
Кислотность. При понижении
рН органические примеси в воде адсорбируются
лучше
Свойства адсорбента.
Отечественной промышленностью выпускаются
активированные угли различных марок,
характеристики некоторых представлены в
таблице.
| Марка |
Поверхность переходных пор м2/г |
| ОУ-А |
138 |
| ОУ-Б |
138 |
| КАД молотый |
64 |
| КАД иодный |
110 |
| АГ-2 |
33 |
| СКТ |
108 |
| АР-3 |
48 |
| БАУ |
50-60 |
| ДАК |
30 |
Сырьем для активированных
углей может быть практически любой
углеродсодержащий материал: уголь, древесина,
полимеры, отходы пищевой, целлюлозно-бумажной и
других отраслей. Прежде чем использовать
активированные угли в аквариумной установке,
нужно убедится в их безопасности. В силу качеств
преобретенных от исходных материалов или
воздействия катализирующих присадок (например:
фосфорной кислоты) угли могут оказать активное
воздействие на кислотные показатели воды. При
введении в технологию каждой новой партии
активированного угля следует сделать
контрольное фильтрование, с замером показателя
рН до и после фильтрования.
Регенерация.
Со временем эксплуатаци
активированные угли насыщаются извлеченными из
воды веществами и тогда наступает необходимость
замены адсорбента. Такое состояние
активированного угля определяется в
соответствии с достижением точки проскока. Точка
проскока это тот момент, когда вода на выходе
перестает отвечать предъявляемым требованиям.
Если у аквариумиста нет возможности измерять
соответствующие параметры, к замене
фильтрующего материала следует подойти с
эмпирических позиций. Например производить
замену активированного угля раз в два месяца с
необходимой коррекцией в дальнейшем. Успех здесь
зависит от наблюдательности и квалификации
рыбовода. Если не производить своевременной
замены угля, он перестает работать как адсорбент
и нечинает исполнять лишь функции механического
фильтра (если фильтрующий слой статичен).
Постоянное использование свежего адсорбента
мероприятие дорогое и поэтому весьма актуален
вопрос регенерации ранее использованного
материала. Это положение справедливо только в
отношении углей изначально использовавшихся в
данном рыбоводном хозяйстве. Ни в коем случае не
использовать угли находившиеся предварительно в
промышленном производстве или с неизвестным
прошлым!
Адсорбированные вещества из угля в промышленном
производстве извлекают несколькими способами. В
аквариумистике не все эти методы достыпны или
доступны частично.
Возможна десорбция насыщенным или перегретым
паром.Температура перегретого пара при этом (при
избыточном давлении 0,3-0,6 МПа) равна 200-300°С.
Для регенерации могу быть использованы
органические растворители - метанол, бензол,
дихлорэтан, метиленхлорид и др. Процесс
проводится без нагревания. По окончании
десорбции остатки рарастворителей из угля
удаляют паром.
Термическая регенерация проводится в печах при
температуре 700-800°С в бескислородной среде.
Термическая регенерация связана с потерей части
адсорбента (15-20%).
Регенерация адсорбента
будет тем более успешна, чем более своевременно и
регулярно она проводится.
** Практическая
часть
Аэрация.
Общепринятое в
аквариумистике понимание значения аэрации для
оборотной аквасистемы в общем-то верно. Основным
агентом в этом процессе является кислород.
Кислород участвует в реакциях окисления, объем и
глубина которых являются залогом жизни не только
в аквариуме, но и на Земле в целом. От содержания в
воде кислорода зависит не только дыхательнная
функция гидробионтов, но и ряд физических
параметров воды как раствора.
Для химических веществ, к
коим относится и кислород в практике принят
параметр растворимости в воде. Растворимость
газов в воде наибольшим образом зависит от
давления газа и температуры воды. В любительской
рыбоводной практике давление газа обычно
опускается, поскольку насыщение воды кислородом
чаще всего ведется по безнапорной технологии и
показатель давления практически неподконтролен
аквариумисту. Температурная составляющая
растворимости кислорода довольно динамична и
хорошо управляема. Градиент растворимости
кислорода в зависимости от температуры воды
достаточно велик.
Растворимость кислорода в чистой воде.
| Температура (°С) |
20 |
22 |
24 |
26 |
28 |
| Растворимость (мгр./л.) |
9,02 |
8,67 |
8,33 |
8,02 |
7,92 |
Одновременно
температура воды влияет и на потребность в
кислороде гидробионтов. Чем выше температура тем
интенсивнее идет обмен веществ в живых
организмах. На поддержание высокой
интенсивности обмена веществ нужно больше
кислорода.
На растворимость кислорода в
воде оказывает влияние соленость. Не редко на
практике в терапевтических или физиологических
целях возникает необходимость введения в воду
поваренной или иной соли. В таблице представлена
динамика зависимости растворимости кислорода от
селености воды.
Растворимость кислорода в чистой воде.
| Соленость при Т 26°С ( ‰) |
0 |
10 |
20 |
30 |
35 |
| Растворимость (мгр./л.) |
8,1 |
7,7 |
7,2 |
6,8 |
6,6 |
Косвенно на уровень
содержания кислорода в воде оказывает влияние
насыщенность органическими и неорганическими
веществами. Кислород извлекается из воды в
результате протекания некотрых неорганических
химических реакций (химическое потребление
кислорода - ХПК). Разложение органического
вещества также требует расхода кислорода
(биологическое потребление кислорода - БПК).
Удаление из аквариума веществ требующих на свой
метаморфоз кислорода, способствует повышению
содержания его в воде. Таким образом организация
вывода из системы кислородактивных соединений
способствует повышению уровня содержания
кислорода в воде.
Переход кислорода в воду
предлагается рассматривать в три этапа.
Переход газообразного
кислорода на границу раздела сред газ - жидкость.
Газообмен идет за счет процессов диффузии и
конвекции и осуществляется сравнительно быстро.
Преход через границу
раздела газ - жидкость. Этот процесс
диффузионный. Диффузия в воде проходит очень
медленно. Диффузия кислорода через
поверхностную пленку определяется прежде всего
химией воды и кислорода. С увеличением
температуры скорость диффузии возрастает.
Примеси поверхностно-активных веществ уменьшают
коэффициент переноса кислорода. Лимитирующая
роль также принадлежит и толщине пленки -
пограничного слоя слоя на разделе вода - газ.
Турбулентность и перемешивание уменьшают
толщину пленки, тем самым повышается скорость
перехода кислорода в воду. Также перемешивание
воды позволяет привлечь в процесс захвата
кислорода водой еще и свойства конвекции,
которая является более кислородактивным
процессом нежели диффузия.
Переход кислорода с
поверхности раздела в жидкость. Процесс
осуществляется главным образом за счет
конвекции.
Для определения
содержания кислорода в воде обычно пользуются
методом Винклера или оксиметром. Оба метода без
особых затрат времени позволяют определить
содержание растворенного кислорода с точностью
0,1 мл/л.
Метод
Винклера.
Реактивы.
Раствор
хлористого марганца MnCl2 4H2O. Растворить 600 г. соли в
дистиллированной воде и довести объем до 1 л.
Щелочно-йодистый
раствор. 320 г .NaOH и 600 г. NaJ растворяют в
дистиллированной водеи после охлаждения доводят
объем до 1 л.
Раствор серной
кислоты H2SO4 . 280 мл концентрированнной серной
кислоты приливают к 500 мл. дистиллированной воды
и после охлаждения доводят объем до 1 л.
Растворимый
крахмал. 1,0 г.разводят небольшим количеством
холодной дистиллированной воды, вливают в 100
мл.кипящей дистиллированной воды и кипятят в
течении 1-3 мин. рствор крахмала должен быть
прозрачным. Его консервируют добавлением
салициловой кислоты (0,15 г/100мл)
Раствор
тиосульфата натрия Na2S2O3 5H2O. 5 г. реактива разводят в 1 л.
дистиллированной воды. Для консервации
добавляют 1-3 мл. хлороформа. использовать
рекомендуется по истечении нескольких дней
после приготовления.
Ход
определения.
В 100 г.
отобранной воды добавляют 1 мл. раствора MnCl2 и 1 мл. щелочно-йодистого раствора. После
этого сосуд с пробой закрывают, так чтобы не
осталось пузырьков воздуха. Проба
перемешивается. Дальнейшая обработка проводится
после того. как образовавшийся в пробе осадок
осядет и будет занимать не более 1/3 объема
склянки.
Не взмучивая
осадка добавит 1 мл. раствора серной кислоты.
Закрыв склянку, чтобы не осталось пузырьков
воздуха перемешать содержимое до полного
растворения осадка. Проба готова к титрованию.
При
непрерывном перемешивании титруют раствором
тиосульфата до тех пор пока проба не станет слабо
желтого цвета. Добавляют затем небольшое
количество раствора крахмала (проба приобретает
голубой цвет). Продолжают титровать до полного
обесцвечивания.
Снимают с
бюретки отсчет с точностью до 0,01 мл.
Вычисление
концентрации раствореного в воде кислорода.
Расчет проводится по формуле
O2=160n/(V-2) мг/л
где n - объем пошедшего на титрование тиосульфата;
(V-2) - истиный объем кислородной склянки за
вычетом воды, вытесненной при добавлении в
процессе фиксации кислорода 1 мл. MnCl2 и 1 мл.
щелочно-йодистого раствора.
При достаточном
опыте можно ориентироваться и по поведению
обитателей аквариума. Рыба не должна плавать
уткнувшись ртом в поверхность воды и не должна
учащенно, жадно "глотать" воду. Улитки
мелании при недостатке кислорода покидают грунт
и собираются на стенках аквариума.
Потребность в кислороде у
разных рыб разная. Кроме того имеется разница в
потреблении кислорода в зависимости от
времени суток, физиологического и
психологического состояния, от возраста рыб.
Существуют понятия летальной и минимально
допустимой величины насыщения воды кислородом.
Минимально допустимая величина насыщения воды
кислородом находится в пределах 3-5 мгр/л.
Гидробионты могут жить при минимальном
показателе кислорода, но они находятся в
условиях риска. Минимальный показатель
насыщения воды кислородом сраведлив для рыб в
спокойном состоянии. Для того чтобы имелся запас
по концентрации кослорода в воде, нужно
обеспечит превышение минимального уровня, здесь
можно рекомендовать 6 мгр/л. Естественно,
повышение содержания в воде кислорода до 100%-го
насыщения обеспечит более комфортный режим
культивирования гидробионтов.
Из принятых в аквариумной
практике методик насыщения воды кислородом
барботаж является самым распространенным и
достаточно эффективным. Хотя барботаж не
позволяет достичь стопроцентного насыщения воды
кислородом, тем не менее поддерживать
физиологически благоприятный режим дли
гидробионтов он позволяет. Конечно здесь не идет
речь о сверхплотных посадках. Кроме
технологической простоты барботаж еще позволяет
использовать кинетическую энергию воздуха для
оборудования эрлифта - воздушного насоса.
Принцип эрлифта используется в аквариумной
практике издавна при изготовлении фильтров.
Эрлифт представляет собой
трубу с открытыми концами в которую нагнетается
воздух.
| Принцип действия насоса
основан на разности между удельным весом воды
окружающей трубу снаружи, и удельным весом
водовоздушной смеси, наполняющей трубу. На
работу эрлифта влияет диаметр трубы, количество
подаваемого воздуха, величина заглубления
насоса, величина подъема воды, размер пузырьков
воздуха, степень шероховатости стенок трубы. |
 |
Повышения количества
кислорода растворенного в воде можно добиться
используя в технологии не воздух, а газообразный
кислород. Еще большего эффекта по насыщению воды
кослородом достигают путем оксигенации.
Однако такой путь технически гораздо более
сложен и требует наличия напорной водороводной
системы. Оксигенация позволяет перешагнуть 100%-й
рубеж насыщения воды кислородом, что в свою
очередь дает возможность применения
сверхплотной посадки и увеличить темпы роста
рыб.
Перенасыщение воды
кислородом и другими газами также как и
недостаток кислорода, отрицательно действует на
рыб. При этом возникает патологическое
состояние, называемое газовой эмболией, которое
вызывается закупоркой пузырьками воздуха
мелких, в основном жаберных, кровеносных сосудов.
Развитие болезни обусловлено быстрой сменой
парциального давления кислорода и других газов
(в основном азота) в воде. Обычно парциальное
давление газов крови рыбы уравновешено с
парциальным давлением газов в воде. При быстром
изменении этого давления может возникнуть
избыток газов в крови и образование пузырьков,
которые являются причиной гибели рыб.
При пременении технологий
создающих насыщение воды газами свыше ста
процентов их растворимости, необходимо
обеспечить медленный процесс повышения
концентрации раствореннных газов.
** Практическая
часть
Температурный режим.
Влияние температуры на
жизнедеятельность любого организма неразрывно
связано с воздействием температуры на течение
химических реакций. Большинство жизненно важных
процессов можно представить как серию
химических реакций, катализируемых ферментами.
При достаточно низких температурах некоторые
принципиально важные для жизнедеятельности
реакции не идут вообще или протекакют слишком
медленно для обеспечения жизнедеятельности
организма. При повышении температуры скорость
химических реакций возрастает. При дальнейшем
увеличении температуры кинетическая энергия
атомов вовлеченных в процесс жизнедеятельности
становится достаточной для разрушения некоторых
необходимых организму соединений. Это уменьшает
скорость химических реакций и приводит к
снижению темпов роста рыбы. При определенных
значениях температуры происходит полное
разрушение жизненно важных химических
соединений, приводящее к гибели рыбы.
Химические реакции в
значительной степени определяют метаболизм
пойкилотермных животных и именно с этой точки
зрения необходимо подходить к вопросам
поддержания температурного режима в аквариуме.
Температурный фактор также
играет определяющую роль и в химии и физике воды
как среды обитания. При повышении температуры
прежде всего уменьшается содержание
растворенного в воде кислорода. Увеличение
температуры влечет сдвиги в аммиачном балансе,
концентрация токсичной формы аммиака NH3
удваивается при возрастании температуры на 10°С.
Повышенные температуры увеличивают общий
аммонийный фон в аквариуме активизируя процессы
превращения азотсодержащих веществ и степень
контакта с ними гидробионтов.
В аспекте тепловодного
аквариума рассматриваются прежде всего
стенотермные гидробионты. Стенотермность
подразумевает определенную требовательность к
температурным параметрам и тем самым задает
достаточно узкую амплитуду термических
колебаний (5-7°С). Значения теператур здесь лежат в
пределах 22 - 30°С. Температурные параметры в
которых обитает рыба в естественной среде
обозначают как температурную валентность вида.
Гидробионтов в известной степени можно
адаптировать и за пределами температурной
валентности, однако нужно учитывать, что тогда
начинают дей ствовать стрессовые факторы и не
типичные инвазии. Таким образом без особой
необходимости при содержании рыб за пределы
температурной валентности выходить не стоит.
В естественной среде
обитания как правило на рыб воздействует фактор
суточных и миграционных температурных
колебаний. Физиология рыб построена в
соответствии такими колебаниями и из
соображений корректного культивирования
животных в искусственных условиях диктует
желательность моделирования процесса изменения
температур в течении суток. В устоявшейся
аквариумной практике к таким мероприятиям как
правило не прибегают, причем достигаются
определенные успехи в аспекте разведения
культивируемых видов. Однако это обстоятельство
вовсе не говорит в пользу пренебрежения фактором
суточных температурных колебаний.
** Практическая
часть
Аквасистемы и рыбоводные емкости.
Рыбоводные системы
практикуемае в аквариумном рыбоводстве чаще
всего сводятся к использованию полузамкнутых
установок. Любой аквариум с режимом регулярной
подмены воды и блоком регенрации
соответствуетопределению полузамкнутой
установки.
Рыбоводные емкости.
Естественно основным
элементом аквасистемы является рыбоводная
емкость. На сегодняшний день получили
распространение емкости из силикатного стекла,
органического стекла и бассейны из металла или
бетона.
Наиболее просты и
сравнительно дешевы аквариумы из силикатного
стела. Простота их сборки и надежность позволяют
довольно быстро оборудовать любое аквариумное
хозяйство. Силикатные аквариумы гигиеничны и
выгодны в декоративном плане. Собираются
силикатные аквариумы по бескаркасной схеме с
применением силиконовых герметиков, которые и
являются в этом случае основным конструкционным
элементом. От физико технических характеристик
герметика зависит качество собранного
аквариума. Герметики поступающие в продажу как
правило сопровождаются аннотацией указывающей
на возможность их использования в аквариумной
практике. Объм аквариума рекомендуемый на
этикетке герметика не совсем точная
характеристика для его прочностных параметров.
Лимитирующим фактором в использовании
материалов используемых для сборки аквариума,
является величина давления создаваемого на
конструкцию и прогибы стекла, а совсем не объем
воды заполняющей емкость. Поэтому если задаться
корректной высотой водного столба можно собрать
аквариум практически любого объема.
Высота аквариума в зависимости от толщины
стекла.
| Высота аквариума (см.) |
30 |
40 |
50 |
60 |
70 |
| Толщина стекла (мм.) |
5 |
6 |
8 |
8 |
10 |
Обязательно нужно обратить
внимание на наличие антисептических присадок в
составе герметика. Такие герметики ни в коем
случае применять нельзя!
Коммерческая сеть сейчас предлагает множество
силиконовых герметиков и привести здесь список
их не представляется возможным. Очень хорошими
характеристиками обладает отечественный
герметик выпускаемый Казанским заводом
синтетического каучука - компаунд
кремнийорганический КЛТ-30 марка "А".
Имеется также вариант
каркасной сборки силикатного аквариума, но эта
технология отошла в прошлое по причине
технологической сложности и ненадежности.
Аквариумы из органического
стекла обычно используются в случае особых
требований предъявляемых к рыбоводной емкости.
Прежде всего такие аквариумы дороже силикатных.
Сборка аквариума из оргстекла технологически
сложный и продолжительный процесс. Оптические
свойства органического стекла явно не высоки
особенно если рассматривать их во времени.
Использование оргстекла в производстве
аквариумов позволяет собирать емкости большой
глубины и сложной геометрической формы,
исполнение такой задачи при применении
силикатного стекла повлечет за собой
значительное удорожание конструкции.
Склейка оргстекла производится посредством
заплавления стыков заготовок органическими,
хлорсодержащими растворителями (трихлорэтилен,
дихлорэтан, хлороформ). Наихудший из вариантов -
использование дихлорэтана. Дихлорэтан и его пары
- сильнейшее отравляющее вещество!
Хорошие результаты дает использование в сборке
аквариумов из оргстекла применение акриловых
масс выпускаемых в стоматологической сфере.
Соединения полученные при их помощи имеют
хорошую крепкость и сравнительно быстро
полимеризуются.
Емкости из металла или
бетона чаще применяются в производственных
целях, хотя существует и вариант оборудования
декоративных бассейнов. Емкости из металла
исполняются из обычной листовой стали Ст3, при
желании можно воспользоваться и марками
нержавеющей стали.
Фильтрация.
Залогом успешного
культивирования гидробионотов конечно же
является правильно организованный баланс между
биотической и абиотической нагрузкой
создаваемой населением аквариума и собственной
востановительной мощностью рыбоводной системы.
Существуют экстенсивный и интенсивный пути
решения этой задачи.
Экстенсивный путь
предполагает увеличение предоставляемого
гидробионтам объема воды. Такой подход самый
примитивный и самый трудный в реализации. Тем не
менее он имеет неоспоримое преимущество -
решается проблема стрессового фактора от
стесненности жизненного пространства.
Интенсивный путь -
организация технологического процесса
регенерации воды. Обеспечить этот процесс
позволяет система фильрации. Фильтры
наполняющие систему фильтрации функционаально
специализированы и в целом в ограниченом объеме
позволяют смоделировать преобразования
вещества в природе. При этом фильтры автономны
как самостоятельные системы и при необходимости
могут быть исключены из общей цепочки
регенерации воды или работать без нее. В
приближенном виде технология регенерации
выглядит так:
Механическая очистка
Биологическая очистка
Адсорбция
Обеззараживание.
Механическая очистка.
Фильтры механической очистки предназначены для
удаления взвешенного вещества из воды поданной
на фильтрацию. Извлечение примесей
обеспечивается прохождением воды через
статичный фильтрующий массив. Эффективность
работы таких фильтров задается фракцией
фильтрующего материала и скоростью проходящей
через тело фильтра воды. Обслуживание таких
фильтров сводится к регулярной промывке или
смене фильтрующего материала.
При определении
конфигурации механического фильтра нужно
исходить из параметров оседания в его теле
отфильтровываемых частиц. Чем мельче поры
механического фильтра тем меньший путь и с
большей скоростью в его теле пройдет частица до
оседания. Однако уменьшать поры фильтра можно до
определенного предела - чем мельче поры тем
большее сопротивление водному потоку они
оказывают. Кроме того фильтр с мелкими порами
требует более частого промывания. Приведенные
предпосылки описываются формулой
Q = AK/d
где Q - расход воды через
фильтр (л/с), A - площадь фильтрующей поверхности (м2),
K - коэффициент проницаемости фильтрующего слоя, d
- толщина фильтрующего слоя (м).
Коэффициент проницаемости К варьирует в
зависимости от количества, размера и характера
взвешенных частиц, содержащихся в фильтруемой
жидкости.
Зависимость коэффициента К от
фракционности наполнителя.
| % вытеснения воды загрузкой фильтра |
45 |
50 |
55 |
| К |
0,60 |
0,50 |
0,40 |
Кроме того, каждая
промывка фильтра также существенно отражается
на величине этого коэффициента.
Сетчатые фильтры. К ним
относятся наверное самые распространенные в
аквариумной практике синтетические губки и
перлоновая вата. Сравнительно дешевы и просты
как в изготовлении так и в эксплуатации.
Гравийно-песчанние фильтры.
Издавна применяются в технологии очистки воды.
Дешевы и надежны. Простота конструкции позволяет
создавать разнообразнейшие конфигурации.
Модификацией гравийно-песчанного фильтра можно
считать грунт нажодящийся в аквариуме.
Диатомовые фильтры.
Конструкции дорогие, но позволяют добиться очень
высокой степени механической очистки воды.
Фильтрация ведется за счет оседания на
всасывающем сетчатом рукаве массы из раковин
диатомовых водорослей. Применение возможно в
напорных фильрующих системах.
Гравитационные фильтры.
Работают на основании того, что частицы
взвешенных примесей имеют большую плотность
нежели вода и под действием гравитационных или
центробежных сил отделяются от движущегося
водного потока. Используюся в аквариумистике
крайне редко из-за громоздкости.
Биологическая очистка.
Биологическая фильтрация в практике регенерации
воды обычно устанавливается следующей ступенью
после механической очистки. Предварительная
механическая очистка позволяет удалить из
водного потока взвешенное вещество которое
забивае тело биологического фильтра и тем самым
препятствует его эффективной работе. Функция
биологического фильтра преобразование и вывод
из оборота растворенного биологического
вещества.
Если ступень механической
фильтрации предусматривается в
гравийно-песчанном исполнении, а биологический
фильтр запроектирован на статичную загрузку, как
правило ступени механической и биологической
очистки совмещаются, по причине относительно
малой механической нагрузки на фильтр. Кроме
этого создается прецендент для экономии места на
оборудование блока фильтрации. За определяющий
здесь берется расчет биологического фильтра.
Адсорбция.
Физико-химическая очистка организуется
следующей ступенью за биологической. После
прохождения тел механического и биологического
фильтров, вода уже достаточно свободна от многих
примесей, которые могли бы довольно быстро
заилить адсорбционные материалы и тем самым
воспрепятствовать процессу физический очистки.
Также на ступень адсорбации возлагается
нагрузка вывода из оборота продуктов
деятельности биофильтра (например: нитратов и
нитритов).
В отдельных случаях
адсорбция может заменить собой биологическую
фильтрацию, но это дорогой путь.
Активированный уголь.
Наиболее распространенный в аквариумной
практике метод адсорбционной очистки воды.
Относительно трудно контролировать активное
состояние адсорбента, следовательно приходится
производить обслуживание загрузки опираясь на
косвенные данные.
Ионообменные колонны.
Позволяют достичь очень высокого уровня очистки
воды. Просты в изготовлении и эксплуатации.
Пеноотделительные колонны.
Растворенное вещество концентрируется на
поверхности пены образованной пузырьками
воздуха вдуваемого в нижнюю часть колонны. Пена
собирается и удаляется. Пенное фракционирование
дает хорошие результаты в солоноватоводных
системах, но применимо и в пресноводных в
присутствии относительно высоких концентраций
органических веществ.
Обеззараживание воды.
Культивирование рыб так или иначе
потенциально сопряжено с опасностью
возникновения инвазий. Обеззараживание
рыбоводной системы в этом свете приобретает
актуальное звучание. Наилучший эффект
обеззараживания достигается в более чистой воде.
Поэтому ступень обеззараживания располагается в
самом конце системы регенерации, где вода
предварительно уже прошла фильтрацию и наиболее
свободна от примесей. Из методик применяемых в
практике водоподготовки для аквариумного
рыбоводства целесообразно выделить:
Озонирование. Технология не
сложная, но имеются издержки которые заставляют
ограничить использование озона. Остаточный озон
выходящий в атмосферу, может накапливаться в
закрытых помещениях и если в них находятся люди
представляет опасность для их здоровья.
Необходимо или оборудовать систему
нейтрализации озона, или использовать его в
помещениях где люди не работают. Технология
получения озона предъявляет определенные
требования качеству исходного сырья, что
также влечет усложнения в конструкции озоновой
установки.
Ультрафиолетовое
облучение. Изготовление и эксплуатация
сложностей не представляют. Необходимо следить
за загрязненностью поверхности колбы УФ-лампы.
Замена воды. Замена
воды относится к мероприятиям обеспечивающим
качество воды в рыбоводной системе. Избежать
регулярной замены части воды без потери
параметров исходно заданных зачастую
невозможно. По приведенной причине мероприятия
по замене воды, следует считать неотъемлемым
звеном в технологии регенерации воды в
аквариумном хозяйстве.
Как правило для подмены
используется вода из питьевой водопроводной
сети, она не несет в себе веществ биогенного
характера и тем самым наилучшим образом отвечает
требованиям регенерации.
Режим замены воды
устанавливается в привязке к физиологии
обитателей аквариума. Замены могут быть
ежедневные на 10%, а могут быть и более редкие с
большим процентом подменяемой воды. Обычно
подмена воды составляет около 30% от общего объема
рыбоводной системы.
Как вариант подмены можно
рассматривать устройство проточной системы.
Здесь необходимо задаться предварительно
объемом воды который желательно сменить в
рыбоводной системе (например: 30% за неделю) и
исходя из него установить величину расхода воды.
Хочется предостеречь от черезмерного увлечения
системами проточной подмены воды (в условиях
городского водопровода) - слишком большой расход
может препятствовать налаживанию общего
биоценоза аквариума и на гидробионтов будет
действовать фактор постоянного стресса.
Конфигурация системы.
Фильтры включаемые в
единый цикл регенерации воды, сами по себе
автономны, что дает возможность конфигурировать
систему достаточно произвольно. Каждый из
фильтров имеет собственные допустимые
эксплуатационные характеристики которые можно
максимально активизировать грамотно
сконфигурировав систему регенерации. В
аквариумной практике в основном используются
три основные схемы регенерации.
Последовательная
схема. Здесь лимитирующим фактором
является биофильтр. Создаются наиболее
корректные условия эксплуатации фильтрующих
ступеней. Для того чтобы усилить в целом
оборотную мощность фильтрации, необходимо
наращивать биофильтр.
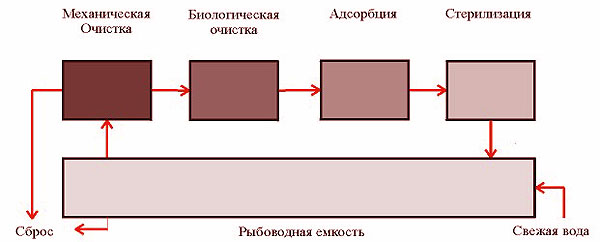
Параллельно-последовательная
схема. Позволяет снять проблемы
лимитирующего фактора биофильтра и максимально
активизировать параметры фильтрующих ступеней
системы.

Параллельная схема.
Фильтрующие ступени работают независимо друг от
друга, эфективность их работы определяется
качеством воды в рыбоводной емкости.
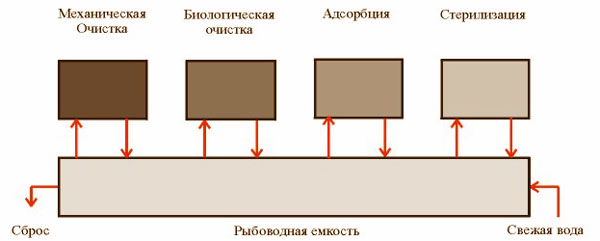
Кроме технологической
конфигурации следует учитывать конфигурацию
конструкционную. Прежде всего нужно отметить
возможность компановки блока регенерации
совмещенно с рыбоводной емкостью. Такое решение
позволяет избежать фактора гидравлического
сопротивления и использовать более дешевые
движетели воды. Недостаток в том, что система
требует отторжения части объема рыбоводной
емкости. Внешнее размещение блока регенерации
позволяет не вторгаться в пространство
рыбоводной емкости, но требует больших усилий в
направлении прекачивания воды.
** Практическая
часть
Инкубационные системы.
При разведении рыб
нередко возникает необходимость отторгнуть
производителей от процесса выхаживания
потомства. Для решения этой задачи используются
устройства называемые инкубаторами.
Устройство инкубатора,
прежде всего должно обеспечивать икре
помещенной в него комфортный кислородный режим.
С этой целью в инкубационную камеру долна
постоянно нагнетаться вода обогащенная
кислородом и имывать икру со всех сторон.
Аммиачный фон в воде
инкубатора должен быть минимальный или вообще
отсутствовать. Перед подачей в инкубационную
камеру вода должна пройти цикл регенерации.
Икра должна подвергаться
физиологически необходимым механическим
манипуляциям. В инкубационной камере должны
отсутствовать "мертвые зоны", в которых икра
залипает и остается неподвижной. Икринки не
должны так же разбиваться черезмерно сильным
перемешиванием.
Сосуд Вейса.
Устройство используется в рыбоводной
практике широко. В основе работы лежит принцип
гашения скорости потока из-за увеличения
площади сечения водовода. Икринки поднимаемые
вверх восходящим потоком доходя до медленно
текущего слоя теряют сообщенную им энергию и
опускаются до встречи с восходящим потоком. |
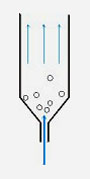 |
Инкубационный
барабан. Икра приводится в движение
посредством перекатывания по внутренним стенкам
барабана во время его вращения. Одновременно при
вращении, через барабан проливается вода. |
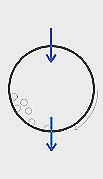
|
Ошибочно понимать
оборудование инкубатора как только устройство
инкубационной камеры которую можно установить в
любом месте рыбоводной установки. Важнейший по
значению момент в аквариумной практике -
инкубирование икры. Соответственно этому
положению определяется и место для инкубатора в
аквариумном хозяйстве. Инкубатор - устройство
состоящее из узла водоподготовки инкубационной
камеры. В узле водоподготовки, вода
обрабатывается перед подачей в инкубационную
камеру. Узел водоподготовки в идеале должен быть
полностью идентичен системе регенерации
оборотной воды в аквариумном хозяйстве. Лучше
когда система инкубатора автономна от
рыбоводного хозяйства, это уменьшает
эпизоотический фон. Если такой возможности нет,
тогда инкубационную камеру можно установить
на выходе блока регенерации воды аквариумного
хозяйства, но здесь будет важно соблюсти условие
выгораживания отдельной емкости для ее
установки.
Определяющим успех моментом
в технологии инкубации икры является
стабильность водных потоков приводящих в
движение икру в инкубационной камере.
Распространенная практика использования для
этих целей эрлифтных насосов порочна изначально.
Эрлифт - насос работа которого зависит от очень
многих факторов и по причине этого не может
считаться стабильной водоподающей системой.
Наилучшим образом для решения задач обеспечения
стабильного водного потока, является применение
водных центробежных насосов (помп). Помпы имеют
стабильную производительность и создают
избыточное водное давление, которое
компенсирует гидравлическое сопротивление
системы водоводов. Особое внимание нужно
обратить на запорную арматуру применяемую для
регулирования напора в инкубационной камере.
Запорная арматура является местом концентрации
и оседания взвешенного вещества и чем более
громоздкий замок в ней используется, тем больше
вероятность ее засорения или падения
давления. Такой недостаток типичен для зажимов
от медицинских капельниц.
** Практическая
часть
© Copyright 1999, Берсенев
Андрей
All Rights Reserved
|
|
|

