Alguns exemplos importantes:
COMPOSTOS HETEROCÍCLICOS
1- Nomenclatura e exemplos
Compostos heterocíclicos são compostos cíclicos contendo, no anel, um ou mais átomos diferentes do carbono. Normalmente, os heteroátomos mais comuns são o nitrogênio, o oxigênio e o enxofre. Na verdade, só consideramos como verdadeiros compostos heterocíclicos aqueles que possuem anéis estáveis. Deste modo, excluímos compostos como, por exemplo, epóxidos e anidridos cíclicos, pois estes compostos sofrem facilmente a ruptura do anel, dando reações que mais se assemelham às reações dos compostos acíclicos.
Não há nenhuma regra rigorosa para a nomenclatura dos heterocíclicos. A maioria deles tem nomes particulares.
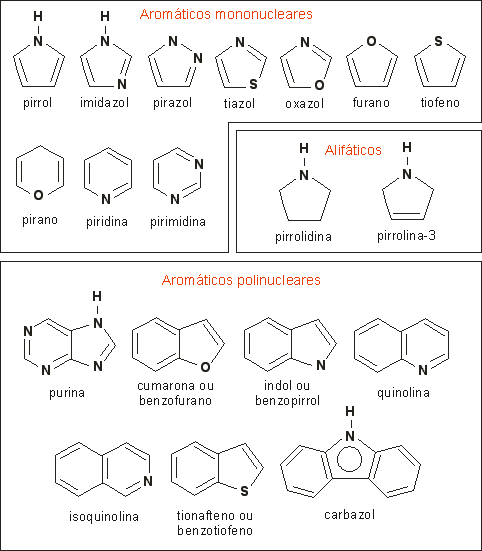
Alguns exemplos importantes:
2- A estabilidades dos compostos heterocíclicos
Os heterocíclicos mais interessantes e mais importantes são os que possuem caráter aromático. Os heterocíclicos aromáticos mais simples são o pirrol, o furano e o tiofeno (veja acima), de anéis pentagonais. A estabilidade destes compostos é explicada da mesma forma que no anel benzênico, através das suas estruturas de ressonância, que conferem grande estabilidade química ao composto. Veja o exemplo do pirrol (as estruturas de ressonância do furano e do tiofeno são análogas às ilustradas abaixo):

Em geral, os heterocíclicos aromáticos dão preferência a reações de substituição eletrofílica: nitração, sulfonação, halogenação, adições de Friedel-Crafts etc (veja aqui os mecanismos destas reações), que mantêm a integridade do anel aromático. Os calores de combustão destes compostos indicam uma energia de estabilização de ressonância de 22-28 kcal/mol, um pouco menor do que a do benzeno (36 kcal/mol), porém, muito maior do que a maioria dos dienos conjugados (3 kcal/mol). A representação dos anéis heterocíclicos aromáticos devem ser representadas, como no benzeno, por um círculo inscrito no anel, indicando a ressonância. Comparativamente, quanto à estabilidade do anel a ao caráter aromático, podemos dizer que: tiofeno >> pirrol >> furano.
3- Propriedades físico-químicas
O tiofeno é um líquido de propriedades físico-químicas muito semelhantes às do benzeno, e constitui inclusive a impureza mais comum no benzeno obtido do alcatrão de hulha. A piridina é um líquido incolor, de cheiro desagradável e bastante solúvel em água. Como foi dito anteriormente, os heterocíclicos aromáticos dão preferência a reações de substituição eletrofílica.
4- Principais ocorrências dos compostos heterocíclicos
Os anéis heterocíclicos são importantes, pois aparecem frequentemente em produtos naturais, como açúcares, hemoglobina, clorofila, vitaminas e alcalóides (cafeína, cocaína, estriquinina etc). Anéis heterocíclicos existem também em medicamentos sintéticos, como os antibióticos (penicilina, amicetina, eritromicina etc)
5- Algumas aplicações dos compostos heterocíclicos
6- Os Alcalóides
Alcalóides são compostos nitrogenados, em geral, heterocíclicos, de caráter básico, que são normalmente produzidos por vegetais e têm ação enérgica sobre os animais - em pequenas quantidades podem servir como medicamentos, e em doses maiores são tóxicos. Quase todos os alcalóides são substâncias sólidas, de sabor amargo. A classificação mais aceita para os alcalóides é aquela que os agrupa de acordo com o núcleo da qual derivam (veja as estruturas moleculares de alguns alcalóides). Os principais grupos de alcalóides são:
6.1) Alcalóides relacionados com a piridina:
Coniina - Encontrada na cicuta, é um dos poucos alcalóides que se apresenta sob a forma líquida. É um veneno fortíssimo.
Piperina - Principal alcalóide da pimenta negra. A toxidez dessa substância é relativamente baixa em relação à dos demais alcalóides.
Nicotina - Principal alcalóide do tabaco, podendo alcançar 4 a 5% da folha seca. O produto puro é um líquido incolor. É um veneno muito violento. Por oxidação pelo dicromato de potássio, dá origem ao ácido nicotínico, que é uma das vitaminas do complexo B.
6.2) Alcalóides do grupo tropânico:
Atropina - Este alcalóide foi isolado da raiz da beladona. É um éster do ácido trópico com o tropanol, com grande aplicação em oftalmologia, devido ao seu poder midriático.
Hiosciamina - É um isômero da atropina, e se encontra em algumas espécies de solanáceas.
Escopolamina - É um epoxi-derivado da atropina.
Cocaína - este alcalóide teve grande importância no início de seu descobrimento, mas está praticamente abandonada como medicamento, devida à grande tendência que apresenta para causar dependência química. A cocaína é um veneno fortíssimo, encontrado na folha da coca, juntamente com outros alcalóides. É um éster do ácido benzóico com um derivado do tropano.
6.3) Alcalóides relacionados com a quinolina:
Quinina - É um pó branco pouco solúvel em água, mas forma sais solúveis, sendo utilizada sob esta forma.
Cinconina - É muito semelhante à quinina em sua estrutura química. Diferencia-se dela porque, em lugar de um grupamento OCH3, apresenta um átomo de hidrogênio.
Estricnina - Em pequenas doses, a estricnina é utilizada como tônico. Em doses elevadas, porém, pode causar a morte.
6.4) Alcalóides relacionados com a isoquinolina:
Morfina - É um sedativo de grande potência e largamente empregado como tal. Por causar dependência, seu emprego é extremamente controlado.
Codeína e Heroína - São também utilizados como narcóticos analgésicos.
Química 2000 - Wagner Xavier Rocha, 1999