PRINCIPAIS MÉTODOS DE OBTENÇÃO DOS ÁLCOOIS
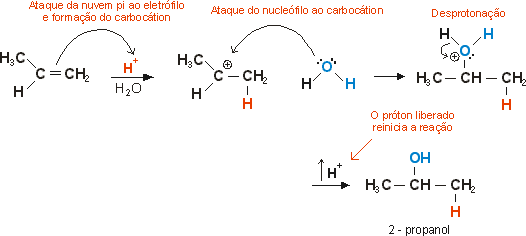
1- Hidratação de alcenos
2-
Hidratação de cicloalcenos
3-
Oxidação branda de alcenos
4-
Hidratação de epóxidos
5-
Reação de aldeídos ou cetonas com reagente de Grignard
7-
Reação de éteres com HX
8-
Hidrólise de ésteres
Em meio ácido, os alcenos reagem com a água formando álcoois:

Os cicloalcenos podem ser hidratados em meio ácido, da mesma forma como os alcenos, produzindo álcoois:

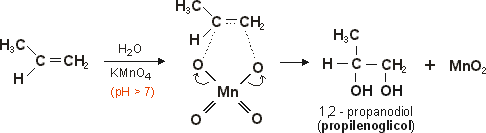
O permanganato em meio neutro ou levemente alcalino é oxidante brando, pois não chega a romper a dupla ligação, mas reage introduzindo oxigênios na cadeia. O permanganato é uma solução de coloração violeta intensa e quando ele passa para MnO2 precipita esse óxido marrom escuro. O resultado da oxidação branda de um alceno com KMnO4 é um diálcool vicinal (glicol). Como exemplo, vejamos a oxidação do propeno:
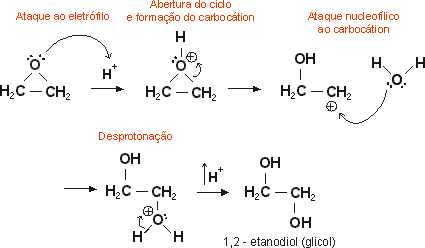
Os epóxidos podem ser hidratados em meio ácido ou básico, produzindo um glicol (diálcool vicinal):
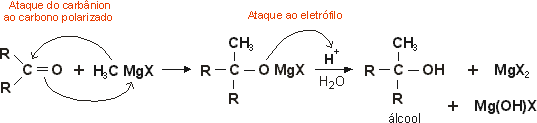
5- Reação de aldeídos ou cetonas com reagente de Grignard
Os aldeídos e cetonas podem reagir com composto de Grignard e posterior hidratação em meio ácido, produzindo álcoois. O reagente de Grignard funciona como doador de carbânion:
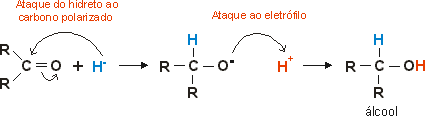
6- Reação de aldeídos ou cetonas com hidreto
Os aldeídos e cetonas podem ser tratados com um agente fornecedor de hidretos (ex: LiAlH4) e posteriormente, tratados em meio ácido. Assim, obtemos um álcool:
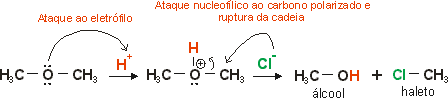
Os éteres, apesar de pouco reativos, podem sofrer ruptura na cadeia, originando dois produtos. A reação com ácidos halogenídricos fortes (HX), por exemplo, fornece um álcool e um haleto. Veja:
Os éteres podem ser hidrolisados em meio básico ou em meio ácido, resultando um álcool e um ácido crboxílico. Em meio básico temos a seguinte proposta mecanística:

Em meio básico a reação é mais rápida, visto que os íons hidróxido adicionados à solução são nucleófilos mais fortes do que a água. Em meio ácido teríamos o seguinte:

Química 2000 - Wagner Xavier Rocha, 1999