
PRINCIPAIS REAÇÕES DOS HALETOS
1- Desalidrificação
2-
Desalogenação de haletos vicinais com zinco
3-
Desalogenação de dihaletos vicinais
4-
Eliminação por nucleófilo em haletos cíclicos
5-
Desalogenação de dihaletos não-vicinais com zinco
6-
Eliminação com sódio metálico em haletos cíclicos
7-
Substituição nucleofílica interna
8-
Reação com alcóxidos
9-
Reação com sais de ácidos carboxílicos
10-
Hidroxilação de haletos aromáticos
Tratando os haletos com uma solução alcoólica aquecida de uma base inorgânica (KOH, por exemplo) é possível transformá-los em alcenos. É importante notar que, no caso de haletos com mais de três carbonos, podem se formar produtos diferentes, em quantidades variadas. No exemplo abaixo, o 2- Bromo butano dá origem a uma mistura de dois alcenos isômeros:

2- Desalogenação de haletos vicinais com zinco
Os dihaletos vicinais, quando tratados com zinco metálico, podem ser desalogenados, originando alcenos. Veja o exemplo abaixo:

3- Desalogenação de dihaletos vicinais
Os dialetos vicinais, quando tratados com OH - em meio alcoólico, sofrem eliminação, produzindo alcinos. Nesse caso, o hidrogênio atacado é o secundário. Veja:

Caso o hidrogênio capturado seja o primário, teremos a formação de dienos conjugados:

4- Eliminação por nucleófilo em haletos cíclicos
Tratando um haleto cíclico com bases pode-se obter um hidrocarboneto alicíclico. Veja:

5- Desalogenação de dihaletos não-vicinais com zinco
Os dihaletos não-vicinais podem ser tratados com zinco metálico, obtendo-se hidrocarbonetos alicíclicos. Veja:

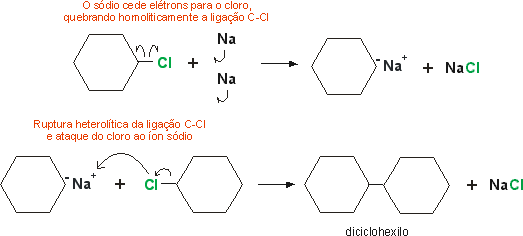
6- Eliminação com sódio metálico em haletos cíclicos
Com sódio metálico, os haletos cíclicos podem produzir hidrocarbonetos alicíclicos binucleados. Veja:
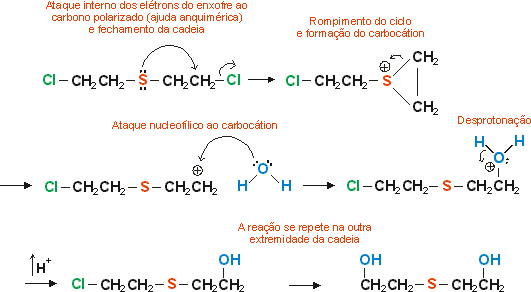
7- Substituição nucleofílica interna
Quando um composto possui em sua molécula um grupo de fácil saída e um nucleófilo, pode ocorrer um tipo especial de substituição nucleofílica. Veja o exemplo abaixo - a hidratação do conhecido "gás mostarda". Nesse caso a reação desse gás com a água é acelerada pela existência do enxofre (nucleófilo), que causa um rearranjo estrutural na molécula, facilitando a saída do cloro. Esse "auxílio" dado pelo nucleófilo interno é chamado ajuda anquimérica.
8- Reação com alcóxidos (síntese de Williamson)
Com alcóxidos os haletos podem produzir éteres:

9- Reação com sais de ácidos carboxílicos
Com os sais de ácidos carboxílicos os haletos produzem ésteres:

10- Hidroxilação de haletos aromáticos
Os haletos aromáticos podem ser hidroxilados, de modo que o ataque nucleofílico ocorra no carbono polarizado da ligação com o haleto, e não capturando um próton. Veja:

Química 2000 - Wagner Xavier Rocha, 1999