[Содержание]
[index]
|
6.4. Получение хинонов окислением
6.4.1. Хиноны из ароматических углеводородов
[6.4.2. Хиноны из замещенных аренов]
6.4.1. Хиноны из ароматических углеводородов
Некоторые ароматические углеводороды можно в определенных условиях окислить до хинонов, являющихся производными п- или о-бензохинона:
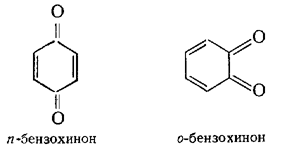 |
(Г.6.25) |
Образование хинонов из углеводородов всегда происходит легче, если двойные связи в a,b-положении к карбонильной группе стабилизированы алкильными и в особенности арильными группами. Так, например, бензол лишь в особо специфических условиях с трудом удается прямо окислить в хинон (с помощью перекиси серебра), антрацен же довольно гладко окисляется в антрахинон, фенантрен - в фенантренхинон; нафталин по окисляемости занимает промежуточное положение. Окисление может быть осуществлено хромовой кислотой, перекисью водорода или кислородом воздуха в присутствии пятиокиси ванадия. При окислении хромовой кислотой в сравнимых условиях были получены следующие продукты:
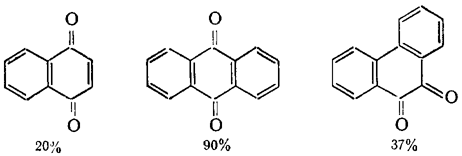 |
(Г.6.26) |
о-Хиноны обладают большим запасом энергии, чем п-хиноны. Поэтому, в частности, фенантренхинон легко окисляется в дифеновую кислоту:
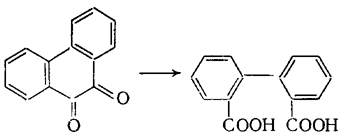 |
(Г.6.27) |
Из нафталина при окислении также получается не только 1,4-нафтохинон, но и фталевый ангидрид (ср. табл. 83 и разд. Г,6.5.1;
промышленное получение фталевого ангидрида).
В приведенной ниже методике окисления углеводородов в хиноны используется большой избыток хромовой кислоты: в противном случае остается непрореагировавшее исходное вещество, затрудняющее очистку. При этом следует прервать реакцию в момент использования всего углеводорода, чтобы предотвратить дальнейшее окисление.
Общая методика получения хинонов из углеводородов действием хромового ангидрида (табл. 89). В трехгорлой колбе на 500 мл, снабженной термометром, мешалкой и капельной воронкой (колба должна сообщаться с внешней атмосферой!), к смеси 0,05 моля исходного вещества (твердое вещество следует тщательно растереть) и 90 мл 90%-ной уксусной кислоты при энергичном перемешивании в течение 1 ч прибавляют раствор 0,25 моля хромового ангидрида в 50 мл 60%-ной уксусной кислоты. Температуру поддерживают в интервале
5-20°С. Затем перемешивание продолжают еще 40-60 мин при 40 °С, чтобы завершить окисление
Для более точного определения конца реакции перед истечением указанного времени каждые 5 мин берут пробу, разбавляют водой, отсасывают, промывают водой Продукт должен быть светло-желтым (не зеленым), а запах углеводорода должен исчезнуть. Можно контролировать, полностью ли израсходовано исходное вещество, быстро определяя температуру плавления 1). По окончании реакции смесь выливают в равный объем воды, отсасывают и перекристаллизовывают.
Таблица 89
Получение хинонов из ароматических углеводородов
| Хинон |
Углеводород |
Т. пл. хинона, °С |
Выход,% |
примечания |
| 1 4-Нафтохинон |
Нафталин |
124 (гексан) |
35 |
|
| 2-Метил-1,4-нафтохинон |
2-Метилнафталин |
106 (метанол) |
45 |
При хранении защищать от света, легко полимеризуется |
| Фенантренхинон |
Фенантрен |
207 (спирт или ледяная уксусная кислота) |
60 |
Неочищенный хинон прокипятить с раствором соды, для того чтобы отмыть кислоту (какую?) |
| Антрахинон |
Антрацен |
285 (диоксан) |
80 |
Конец реакции можно не определять: добавив хромовый ангидрид, нагревать 4 ч с обратным холодильником |
| Аценафтохинон |
Аценафтен |
261 (тетралин) |
50 |
Неочищенный продукт реакции кипятить с тетралином, профильтровать горячим |
[6.4.2. Хиноны из замещенных аренов]

|


