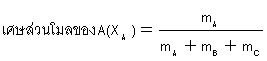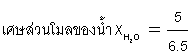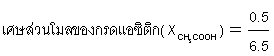|
สารละลาย (Solution = solute + solvent)เป็นสารเนื้อเดียวที่เกิดจากสารอย่างน้อย 2 ชนิดมาผสมกัน
สารละลายที่ได้มีทั้ง 3 สถานะ คือ ของแข็ง ของเหลว และก๊าซ |
|
ความเข้มข้นของสารละลายร้อยละ |
|
ร้อยละโดยมวลต่อปริมาตร
หมายถึง มวลของตัวถูกละลายที่ละลายอยู่ในสารละลาย 100 หน่วยปริมตร โดยทั่วไป
ถ้ามวลของตัวถูกละลายมีหน่วยเป็นกรัม สารละลายมีหน่วยเป็นลูกบาศก์เซนติเมตร
และถ้ามวลของตัวถูกละลายเป็นกิโลกรัม ปริมาตรของสารละลายจะเป็น ลูกบาศก์เดซิเมตร
เช่น สารละลาย CuSO4 เข้มข้นร้อยละ 10 โดยมวลต่อปริมาตร
หมายความว่า ในสารละลาย 100 cm3 จะมี CuSO4 ละลายอยู่
10 g
|
|
โมลต่อลูกบาศก์เดซิเมตร หรือ โมลาริตี (Molarity)
|
โมลต่อกิโลกรัม หรือ โมแลล (Molal)
|
|
เศษส่วนโมล (X)เป็นหน่วยบอกความเข้มข้นที่บอกถึง สัดส่วนโดยจำนวนโมลของสารองค์ประกอบ
ชนิดใดชนิดหนึ่งต่อจำนวนโมลรวมของสารทุกชนิดในสารละลาย ใช้สัญลักษณ์ X
เช่น
|