Alguns exemplos importantes:
FENÓIS
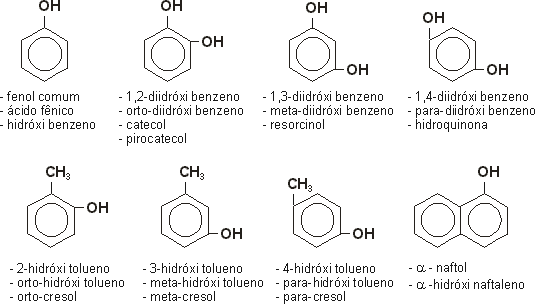
1- Nomenclatura e exemplos
Os fenóis não seguem nenhuma regra fixa de nomenclatura. Os mais simples, no entanto, podem ser nomeados usando o anel aromático como cadeia principal e os grupos ligados a ele como radicais.
Alguns exemplos importantes:
OBS: Três hidroxilas também propiciam três isômeros: pirogalol, floroglucinol e oxiidroquinona.
2- Propriedades físicas
Os fenóis mais simples são líquidos ou sólidos de baixo ponto de fusão e ponto de ebulição elevado, devido à ligação das moléculas, umas às outras, por ligações de hidrogênio. São, em geral, pouco solúveis ou insolúveis em água, de cheiro forte e característico. São tóxicos e têm ação cáustica sobre a pele. A menos que exista na molécula algum grupo susceptível de produzir cor, os fenóis são incolores. Se oxidam facilmente, como as aminas, e muitos fenóis apresentam cor devido à presença de produtos de oxidação corados.
A comparação das propriedades físicas dos nitrofenóis isômeros faz ressaltar um aspecto importante. Veja:
| isômero | PE (a 70 mmHg) | solubilidade | volatilidade em vapor d'água |
| orto-nitrofenol | 100o C | 0,2 g /100g de H2O | volátil em vapor d'água |
| meta-nitrofenol | 194o C | 1,35 g /100g de H2O | não volátil em vapor d'água |
| para-nitrofenol | decompõe-se | 1,69 g /100g de H2O | não volátil em vapor d'água |
Notamos que o orto-nitrofenol tem ponto de ebulição bem mais baixo e muito menor solubilidade em água que os outros isômeros, além de ser o único facilmente destilável em corrente de vapor d'água. Como se explica essas diferenças?
Consideremos primeiramente os isômeros meta e para. Eles têm pontos de ebulição mais elevados devido à existência de ligações de hidrogênio intermoleculares. A solubilidade mais elevada se deve à formação de ligações de hidrogênio com as moléculas de água. A destilação em corrente de vapor depende da substância apresentar apreciável pressão de vapor à temperatura de ebulição da água. A existência de ligações de hidrogênio intermoleculares impede a evaporação dos isômeros meta e para que, portanto, não destilam.
Observando-se o isômero orto-nitrofenol em um modelo molecular, podemos ver claramente que a pequena distância dos grupos NO2 e OH e as suas disposições no anel favorecem a formação de ligações de hidrogênio intramoleculares, ou seja, uma ponte de hidrogênio dentro da molécula. Neste isômero, portanto, as ligações de hidrogênio intramoleculares tomam o lugar das ligações de hidrogênio intermoleculares.
3- Métodos de obtenção
Muitos fenóis simples como o fenol comum, os naftóis e os cresóis podem ser obtidos diretamente do alcatrão da hulha. Por isso, em laboratório, as reações geralmente objetivam a produção de fenóis com estruturas mais complexas.
Veja aqui os principais métodos de obtenção dos fenóis
4- Propriedades químicas
Os fenóis têm caráter relativamente ácido, porém, menos ácido que os ácidos carboxílicos (veja a comparação da força ácida destes compostos). Os fenóis podem ser facilmente diferenciados dos álcoois por meio de alguns testes simples em laboratório.
Veja aqui as principais reações dos fenóis
5- Sais de fenóis
Como já foi dito, os fenóis são compostos relativamente ácidos, e podem ser convertidos nos respectivos sais por soluções aquosas de hidróxidos. Estes sais são conhecidos como fenóxidos ou fenolatos. Como seria de se esperar, os fenóis e seus sais têm características opostas, quanto à solubilidade: os sais são solúveis em água e insolúveis em solventes orgânicos.
A força ácida dos fenóis e a solubilidade dos respectivos sais em água podem utilizar-se tanto em análise quanto em separações. Uma substância insolúvel em água, solubilizada por soluções aquosas de hidróxido, mas não por soluções aquosas de bicarbonato, tem, por força, de ser mais acídica que do que a água, mas menos acídica do que os ácidos carboxílicos; a maioria dos compostos neste escalão de acidicidade são fenóis. Com base na solubilidade em meio alcalino, podem separar-se os fenóis dos compostos não acídicos; por meio da insolubilidade em bicarbonato é possível separá-los dos ácidos carboxílicos.
6- Aplicações dos fenóis
Os fenóis encontram diversas aplicações práticas, tais como:
Entre os diidroxifenóis, a hidroquinona é a mais importante. A partir dela se produz as quinonas, que são compostos coloridos, variando do amarelo ao vermelho. Não apresentam caráter aromático, sendo foretemente insaturados. A ação redutora da hidroquinona, que à temperatura ambiente age com grande rapidez sobre os sais de prata, faz dela um revelador fotográfico de largo emprego.
Enfim, numerosos derivados do fenol estão difundidos na natureza. Entre estes o eugenol e o isoeugenol, que constituem essências de cravo e noz-moscada.
Química 2000 - Wagner Xavier Rocha, 1999