[8.1.Жидкое состояние]
[8.2.Давление насыщенного пара]
[8.3.Определение молекулярной массы]
8.4.Растворы жидкостей в жидкостях
[8.4.1.Законы Рауля]
[8.4.2.Фракционная перегонка]
[8.4.3.Неидеальные растворы]
[8.5.Несмешивающиеся жидкости
Перегонка с паром]
[A-Level-8.rar.zip] Архив (127K)
[index]
8.4.1.Законы Рауля
Раствор - это гомогенная (т. е. однородная) смесь двух веществ. При растворении одной жидкости в другой давление насыщенного пара раствора зависит от давлений насыщенных паров компонентов и от состава смеси. Один из способов выражения состава смеси жидкостей - задание молярной доли каждой из них. По определению:
Молярная доля А в смеси А и В = (Число моль А):(Общее число моль)
или, вводя обозначения молярной доли (мол. доли) через х:
xA = (nA):(nA + nB)
Пар над смесью жидкостей А и В содержит обе эти жидкости. Согласно закону Рауля (1882- 1888 гг.):
давление насыщенного пара каждого из компонентов в смеси равно произведению мол. доли этого компонента на давление насыщенного пара над чистым компонентом, т. е.:
pA = xA(ж) p0A,
где pA - давление насыщенного пара А; p0A - то же над чистым компонентом; xA(ж) - мол. доля А в растворе.
Аналогично для компонента В:
pB = xB(ж) p0B,
Закон Рауля относится к смесям веществ близкой природы, которые, как условились, образуют идеальные растворы. Вещества А и В образуют идеальный раствор, если молекулярные силы А...А, А...В и В...В равны, так что ни объем, ни энтальпия (теплота) не претерпевают изменений при смешении.
Состав пара над смесью жидкостей отличается от состава жидкости. Если xA(п) и xB(п) - мол. доли компонентов в паре, то:
(xА(п)):(xB(п)) = (pA):(pB) = (xA(ж) p0A):(xB(ж) p0B)
Если А более легколетучий компонент нежели В, то p0A &qt; p0B и:
(xА(п)):(xB(п)) &qt; (xA(ж)):(xB(ж))
следовательно, пар обогащается по сравнению с жидкостью более летучим компонентом, т. е. компонентом А (Первый закон Д. П. Коновалова (1881-1884 гг.)).
П р и м е р. При. 80°С давление пара над бензолом равно 10,0•104 Нм-2, а над метилбензолом 4,0•104 Нм-2. Необходимо найти мол. долю метилбензола в паре, равновесном с жидкой смесью бензола и метилбензола при 80°С при условии, что мол. доля метилбензола в растворе равна 0,60.
Р е ш е н и е.
(Количество метилбензола в паре):(Количество бензола в паре)=
(0,60/0,40)•(4,00•104/10,0•104) = 0,60
Мол. доля метилбензола = (Число моль метилбензола : Общее число моль) =
0,60/1,60 = 0,375

Рис. 8.7. Кривая в координатах Р - х для идеальной смеси жидкостей:
1 - кривая общего давления пара; 2 - кривая состава пара; 3 - соединительная линия (нода)
На рис. 8.7 приведены некоторые результаты вычислений подобного рода для идеальных смесей А и В различного состава. Общее давление насыщенного пара есть сумма парциальных давлений паров рA+pB. Если общее давление пара есть робщ, то состав жидкости характеризуется точкой Ж, а состав пара - точкой П; линию П - Ж называют соединительной. По сравнению с жидкостью пар обогащен более легколетучим компонентом А. На рис. 8.7 различие в составах пара и жидкости для наглядности преувеличено.
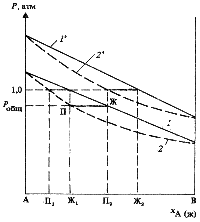
Рис. 8.8. Кривая в координатах Р - х для температур Т1 и T2:
1,1' - составы жидкостей при Т1 и T2;
2,2' - составы паров при Т1 и T2
На рис. 8.8 приведены Р - х - кривые для двух температур Т1 и Т2. Жидкость закипает тогда, когда давление ее паров достигает атмосферного давления. Жидкость состава Ж1, закипающая при температуре Т1, равновесна с паром состава П1, а жидкость Ж2, закипающая при температуре Т2, равновесна с паром состава П2. Все эти параметры могут быть отображены графически в координатах Tкип - х.
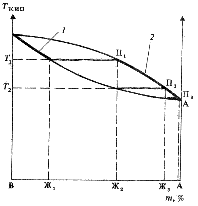
Рис. 8.9. Кривая в координатах Tкип - m для идеальной смеси жидкостей:
1 - линия состава жидкости; 2 - линия состава пара
Температура кипения изменяется с составом постепенно. Ни линия жидкости, ни линия пара не являются прямыми - даже для идеальных смесей.
Если состав выражен не в мол. долях, а в масс. долях или в процентах по массе, то все равно кривые зависимости Tкип - х имеют одинаковый вид (рис. 8.9), так как:
Содержание А, % (масс.) = 100•масс. доля А.
[8.4.2.Фракционная перегонка]
[index]