|
Explanaremos o assunto seguindo a
seqüęncia dos itens apresentados no quadro abaixo.
1 - Introduįão
2 - Hemostasia primária
3 - Hemostasia secundária
. Mecanismo da coagulaįão
. Anticoagulaįão
. Fibrinólise
|
1 - Introduįão
A hemostasia é um complexo mecanismo desencadeado pelo organismo para coibir uma hemorragia.
Ela se passa nos vasos de pequeno calibre (arteríola terminal , vęnula pós-capilar e capilar)
e para que tenha sucesso, é necessário que construa um tampão (trombo hemostático) na altura da
lesão vascular.
Para a formaįão do trombo hemostático participam as plaquetas, inúmeras substâncias do sangue
circulante e a própria parede vascular no local da lesão.
Mostramos na Figura 1 os primeiros acontecimentos para a formaįão do referido trombo.

Figura 1: Início da formaįão do trombo hemostático.
Como é visto na figura 1, as plaquetas (em azul) aderem ā fibrila de colágeno (adesividade
plaquetária) e, para que a adesividade seja estável, é importante a interaįão com o fator "von
Willebrand" (glicoproteina de adesividade).
Após a adesividade, outras plaquetas vão aderir ās plaquetas unidas ao colágeno formando um
aglomerado (agregaįão plaquetária).
Esse processo se faz em poucos segundos e costuma-se designa-lo por hemostasia primária,
reservando-se a expressão hemostasia secundária para a ativaįão dos fatores que levam ā
formaįão da trombina e, conseqüentemente, da fibrina. Este segundo processo demora vários
minutos para ser completado e é de suma importância porque, para que o trombo hemostático
primário seja efetivo, ele deverá ser consolidado pela aįão da trombina e pela participaįão
da fibrina.
Devemos ter em mente que essa subdivisão é puramente didática pois, há interdependęncia e
simultaneidade na participaįão das plaquetas, dos fatores plasmáticos e da parede lesada do
vaso.
2 - Hemostasia primária
Antes de entrarmos nesse tópico, vamos falar, resumidamente, da estrutura da plaqueta sob o
ângulo da microscopia eletrônica; assim, ficará mais fácil entendermos as explicaįões que se
seguem. Ver Figura 2
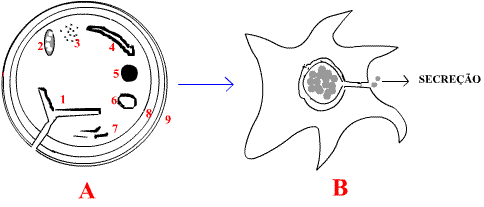
Figura 2: A = PLAQUETA NÃO ATIVADA - 1 = Sistema canalicular aberto.
2 = Mitocôndria. 3 = Grânulos de glicogęnio.
4 = Sistema tubular denso. 5 = Corpo denso. 6 = Grânulo alfa. 7 = Microfilamentos.
8 = Microtubulos circunferenciais. 9 = Membrana plaquetária. Entre a membrana plaquetária
e os microtubulos circunferenciais há os filamentos submembranas. B = PLAQUETA ATIVADA -
Deformaįão das plaquetas e contraįão dos microtubulos circunferenciais e dos filamentos
submembrana com fusão dos grânulos. Detalhes no texto.
Na Figura 2 vemos as alteraįões das plaquetas após sua ativaįão. Em A está representada uma
plaqueta, com sua forma discóide, antes da ativaįão. Podemos identificar, pela microscopia
eletrônica, diversas organelas e, particularmente, os grânulos a e os corpos densos, que contęm
várias substâncias que serão liberadas para o plasma através do sistema canalicular aberto.
Os corpos densos contęm: cálcio, serotonina, ATP e ADP. Os grânulos alfa contęm: fator von
Willebrand, fibronectina, fibrinogęnio, ß-tromboglobulina, trombospondina, fator de
crescimento derivado da plaqueta (PDGF), fatores da coagulaįão V e VIII e uma proteína
neutralizadora de heparina (fator 4 plaquetário).
Em B está representada a plaqueta após ativaįão, que será descrito a seguir.
Após ativaįão, as plaquetas sofrem metamorfose, ou seja, tomam a forma esférica, irregular, com
grandes pseudópodes. Os microtubulos circunferenciais e os filamentos submembranas se contraem,
comprimindo os diversos componentes dispersos no citosol. Com isso, esses elementos são
espremidos e formam uma massa no centro da plaqueta acarretando a eliminaįão de diversas
substâncias pelo sistema canalicular aberto, em especial, as contidas nos corpos densos e nos
grânulos alfa.
Além das plaquetas, a célula endotelial vascular participa intensamente para que se realize o
trombo hemostático primário. Numa citaįão de Mannucci e Remuzzi, uma protease, a
metaloproteinase, cliva fisiologicamente o vWF. Essa protease degrada os multímeros
de tamanho "ultra-grande" de vWF, armazenados nos corpos de Weibel-Palade das células
endoteliais vasculares. A aįão da metaloproteinase gera fragmentos de pequeno, médio e grande
tamanhos que vão compor a molécula do Fator von Willebrand (vWF), que por sua vez é secretado
para o sangue e para o subendotélio.
No subendotélio o depósito desse fator forma a matriz que concorre para a adesividade das
plaquetas.
Para complementar os dados referentes ās plaquetas e ao subendotélio, vamos fazer comentários
sobre os receptores que tomam parte na funįão plaquetária, primeiro na adesividade ao colágeno
(Figuras 3 e 5) e, posteriormente, na agregaįão plaquetária.
Os componentes desses receptores são glicoproteinas que se associam formando complexos.
|
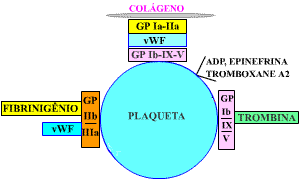
Figura 3: Participaįão dos receptores plaquetários e do colágeno: GP Ia/IIa = receptor da fibrila
de colágeno (específico para a plaqueta). vWF = Fator von Willebrand. GP Ib/IX/V = receptor da
plaqueta para o vWF. GP IIb/IIIa = receptor da plaqueta para o vWF e para o fibrinogęnio.
GP Ib/IX/V = receptor da plaqueta para a trombina. Detalhes no texto. |
|
Na Figura 3 podemos ver que o complexo GP Ia/IIa funciona como receptor da fibrila de colágeno
para o vWF.
Já os complexos GP Ib/IX/V e IIb/IIIa são os receptores plaquetários para o vWF. Desse modo, o
vWF serve de ponte entre os citados receptores promovendo, assim, a adesividade da plaqueta ao
colágeno que foi exposto após a lesão do endotélio. Nesse momento em que a plaqueta adere ao
colágeno, ela é ativada e libera, além de outras substâncias, o ADP que é um ativador
plaquetário.
Por outro lado, o complexo GP Ib/IX/V, também é receptor para a trombina, enzima que promoverá
a ativaįão plaquetária juntamente com o ADP e que comentaremos no item hemostasia secundária,
pois a trombina é gerada após ativaįão do mecanismo da coagulaįão.
Bonnefoy e colaboradores mostraram que o fibrinogęnio também pode mediar a adesividade das
plaquetas ā uma superfície e entre as plaquetas. O fibrinogęnio solúvel somente propicia a
agregaįão das plaquetas quando estas estão ativadas pelos agonistas, tais como o ADP e a
trombina. O receptor das plaquetas para esse fim é a GP IIb/IIIa.
Assim, o fibrinogęnio faz uma ponte entre os receptores GP IIb/IIIa de duas plaquetas. Esse
receptor também é usado pelo fibrinogęnio adsorvido em superfície porém, essa ligaįão, ao
contrário da anterior, não requer a ativaįão plaquetária.
Queremos destacar que a ligaįão das substâncias citadas aos respectivos receptores, e a de
outras substâncias não citadas, se dá com maior ou menor facilidade na dependęncia de um
mecanismo, que vem sendo estudado intensamente, conhecido como "shear rate/stress".
"Shear rate" corresponde ā interface do sangue circulante com a parede vascular. Em outras
palavras, é a velocidade de deslocamento da lâmina de sangue circulante, mais próxima ā parede
do vaso. As plaquetas dessa camada de sangue são, justamente, aquelas que entrarão em contato
com o subendotélio exposto após a lesão do endotélio.
"Shear stress" representa a forįa de colisão das plaquetas entre si e da plaqueta com uma
superfície, por exemplo, a fibrila de colágeno. No fenômeno de "shear rate" as plaquetas são
arrastadas em uma superfície; já no "shear stress" elas se chocam com a superfície.
É importante ressaltar que esse segundo fenômeno verifica-se mais intensamente quando existe
formaįão de turbilhão. Acontece com freqüęncia em casos patológicos, quando há formaįão de
placas de ateroma ou quando há estrangulamento da luz do vaso.
Como mencionamos anteriormente, o "shear rate/stress" aumenta ou diminui a capacidade de uma
substância ligar-se ao seu receptor. Quando diversas substâncias tęm a propriedade de ligaįão
a um mesmo receptor, a variaįão do grau do "shear rate/stress" facilitará ou dificultará a
ligaįão de cada substância.
Como exemplo, citamos a interaįão do vWF com o complexo GP Ib/IX/V que é facilitada com a
intensificaįão do "shear rate/stress".
Outro exemplo é a ligaįão entre duas plaquetas pelo fibrinogęnio e o receptor GP IIb/IIIa que
fica facilitada pelo "shear stress" fisiológico.
Maiores detalhes serão fornecidos pelos trabalhos apresentados em Bibliografia Consultada onde,
com um simples clique, vocę obterá o texto integral.
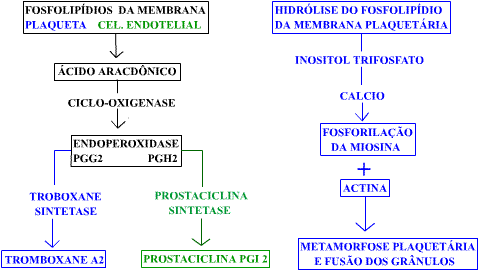
Figura 4: Esquema das reaįões bioquímicas que levam ā geraįão de
Tromboxane A2, de Prostaciclina e ativam a actina e a miosina, responsáveis pela contraįão
dos microtubulos circunferenciais e dos filamentos sub-membrana. Detalhes no texto.
Decorrente da aįão do colágeno, do ADP e da trombina, ocorrem tanto na membrana
plaquetária quanto no seu interior, diversas reaįões que conduzem ās transformaįões
físico-químicas referidas anteriormente. Na Figura 4 destacamos duas dessas reaįões: a primeira,
promove a geraįão de tromboxane A2 pela plaqueta que leva ā agregaįão plaquetária
e de prostaciclina (PGI2), pela célula endotelial, que tem aįão inversa; a segunda reaįão
produz a metamorfose plaquetária que inclui a fusão dos grânulos, e de outros componentes,
com a conseqüente secreįão de diversas substâncias que participam do mecanismo
hemostático (uma delas é o ADP).
Na primeira reaįão, o ácido aracdônico é liberado de dois fosfolipídios da membrana -
fosfatidilinositol e fosfatidilcolina. Essa liberaįão depende da aįão das enzimas das membranas
da plaqueta e da célula endotelial, - fosfolipase C e fosfolipase A2 que são ativadas quando as
substâncias, acima referidas, se ligam aos receptores correspondentes. Com a participaįão da
enzima ciclo-oxigenase, são produzidas as endoperoxidases.
Até esse ponto as reaįões são comuns, tanto para as plaquetas quanto para as células endoteliais;
daí em diante, nas plaquetas, forma-se o tromboxane A2 com a participaįão da enzima
tromboxane-sintetase, e nas células endoteliais, é formada a prostaciclina com a participaįão
da prostaciclina-sintetase.
Na segunda reaįão, as alteraįões morfológicas plaquetárias decorrem da participaįão da
miosina e da actina, proteínas responsáveis pela contraįão plaquetária e a conseqüente
secreįão já referida.
Além dessas duas reaįões, é importante assinalar que o ADP liberado pela plaqueta promove
alteraįão da conformaįão do complexo de glicoproteinas IIb/IIIa o que permite a ligaįão do
fibrinogęnio ao referido complexo e, conseqüentemente, a união entre plaquetas (agregaįão
plaquetária).
Com o exposto, já temos os elementos, importantes, para desenhar o trombo hemostático primário
e apresenta-lo na Figura 5.

Figura 5. Trombo hemostático primário completo.
Detalhes no texto.
Como vemos na Figura 5, o trombo hemostático primário está formado pelas plaquetas aderidas ā
fibrila de colágeno tendo como ligante (seta 2) GP Ia/IIa do colágeno, vWF como ponte e GP
Ib/IX/V da plaqueta (adesividade plaquetária). As plaquetas estão aderidas umas ās outras pelo
ligante (seta 1) GP IIb/IIIa das plaquetas tendo o fibrinogęnio como ponte (agregaįão
plaquetária).
Ressaltamos que esse trombo não está completo para uma hemostasia efetiva e que pode
desfazer-se com facilidade. Para que ele seja completado (consolidado), são imprescindíveis
as participaįões dos mecanismos de coagulaįão, anticoagulaįão e fibrinólise que descreveremos
a seguir.
3 - Hemostasia secundária
Considera-se como hemostasia secundária as ativaįões dos mecanismos de coagulaįão,
anticoagulaįão e fibrinólise que vão atuar no trombo hemostático primário para torna-lo
estável.
Esses tręs sistemas são compostos por substâncias na forma inativa e, para atuarem, necessitam
ser ativadas. Para representar qualquer substância na forma ativada, usamos a letra minúscula
"a". Exemplo: a forma inativa do fator X é representada por FX e a ativa por FXa.
Outra nota de valor é a de que os fatores II, VII, IX e X, ao serem fabricados no fígado,
necessitam da Vit. K para torna-los aptos na ligaįão aos fosfolipídios com o auxílio do cálcio
e, desse modo, poderem agir.
No fígado, no momento da síntese desses fatores, uma carboxilase que depende da Vit. K,
cataliza uma reaįão de adiįão de um grupo carboxil em um resíduo de ácido glutâmico o que faz
com que esses fatores passem a ter dois resíduos de ácido carboxiglutâmico. A importância disso
é que esse duplo resíduo de ácido carboxiglutâmico liga-se ao cálcio que, por sua vez, é o
responsável pela ligaįão do fator ā superfície fosfolipídica carregada negativamente. Isso torna
possível a atividade biológica do fator ativado.
É precisamente nesse ponto que os antagonistas da Vit. K (como o varfarim) atuam.
Os referidos sistemas atuam concomitantemente, e permanecem em equilíbrio dinâmico nos estados
de normalidade.
Como veremos, as reaįões de ativaįão se passam em grupos de poucas substâncias que denominamos
por complexos. Esses complexos estão sempre associados a uma superfície - da fibrila de
colágeno, da célula endotelial, da plaqueta ou do monócito.
A finalidade principal dessas reaįões é a de gerar trombina, que será imprescindível na
ativaįão das plaquetas que formam o trombo primário, na geraįão de fibrina que reforįa o trombo
hemostático e na ativaįão dos fatores V, VIII e XIII.
É importante destacar dois setores da circulaįão sangüínea onde as substâncias dos mecanismos
da coagulaįão, da anticoagulaįão e da fibrinólise, bem como as plaquetas, se comportam de forma
diferente - o do sangue circulante, onde as substâncias e as plaquetas estão na forma inativa,
e no local da injúria vascular (micro-ambiente hemostático), onde elas são ativadas.
Continuar |
Retornar ao índice

|






