3. Orientaįão para o estudo citológico do linfonodo pelo imprint.
Coleta do material e confecįão do imprint:
O linfonodo escolhido para ser biopsiado, deve ser aquele que aumentou no início da
doenįa. Linfonodos de pequeno tamanho na periferia da massa ganglionar, ou que aumentaram
recentemente, podem não levar ao diagnóstico. O cirurgião deve evitar laceraįões do linfonodo,
o que conseguirá tracionando-o por meio de fio de sutura e não com pinįa.
Após a retirada, o linfonodo é colocado sobre gaze embebida em soro fisiológico (jamais
seca). Caso haja muito sangue, deverá ser enxugado com leve toque com gaze. Em seguida, faz-se
um corte com bisturi no sentido sagital do linfonodo. Uma das partes é colocada sobre a gaze
com a superfície voltada para cima (figura 4). Segurando uma lâmina de vidro por uma das
extremidades, fazemos leve toque na superfície do corte com o cuidado para não deslizar
(esfregar). Caso o material ocupe pequeno espaįo na lâmina, podemos repetir a manobra quantas
vezes forem possíveis. Após secar o material, é feita coloraįão com May-Grünwald-Giensa.
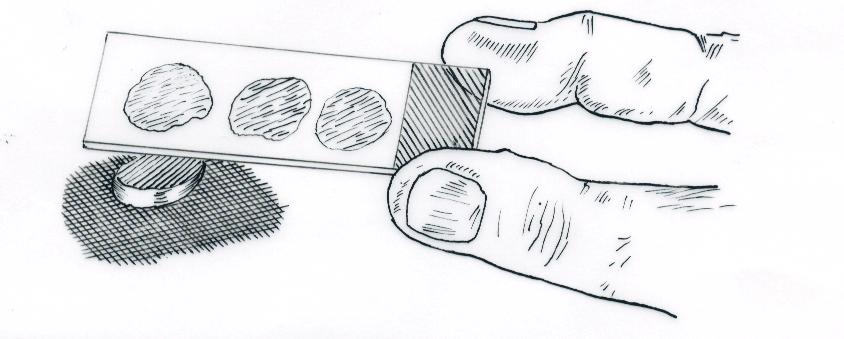
Figura 4: Obtenįão do "imprint". Lâmina com material de tręs "imprints".
Estudo do material obtido pelo imprint:
Ao iniciarmos a leitura devemos percorrer a lâmina usando o pequeno aumento para
avaliarmos a qualidade do material. Consideramos de boa qualidade o material constituído de
fina camada (sem células superpostas) e com poucas hemácias.
Devemos ressaltar que muitas vezes as falhas no material (espaįos vazios) e a citólise,
que dão a impressão de defeito na operaįão, podem corresponder a zonas do linfonodo com tecido
fixo que não se desprende ao toque (fibrose, granuloma, necrose, etc.).
Para leitura do imprint, temos que ter em mente os diferentes tipos de células que
aparecem no linfonodo reacional e o respectivo posicionamento no órgão. Por esta razão,
destacaremos agora as características morfológicas das células citadas anteriormente.
Distribuiįão das células no material obtido pelo imprint.
a) Distribuiįão das células na zona folicular:
Como dissemos, os folículos primários são constituídos por pequenos linfócitos B
"virgens" (com IgD,M de superfície) e por linfócitos T4.
Os folículos secundários, que freqüentemente reconhecemos no imprint do linfonodo
reacional, apresentam um manto com células do folículo primário e uma parte central com células
B em transformaįão (centro germinativo). As células encontradas no centro germinativo variam em
número de acordo com a idade do folículo (tempo a partir do estímulo antigęnico) e do tipo de
reaįão. Nos centros germinativos com poucos dias do estímulo predominam as células linfóides
blásticas e os centrocitos. As células linfóides blásticas tęm pequena faixa de citoplasma muito
basófilo, núcleo redondo, cromatina delicada granulosa e hipocrômica com 2 a 3 nucléolos.
Com o passar do tempo diminuem as células blásticas e aumentam os centrocitos. Os centrocitos
tęm tamanho intermediário entre o linfócito e o centroblasto. O núcleo contém muitas vezes uma
cisura que não ultrapassa o tamanho do raio. Ao invés de cisura podemos ver apenas pequena
reentrância e irregularidade do núcleo (retificaįões e angulaįões). O nucléolo é pouco visível
e o citoplasma é estreito e pouco basófilo, ou não é notado.
Nesse local também são vistos pequenos linfócitos que na maioria das vezes são T4,
poucos plasmócitos e raros imunoblastos. Também podem ser vistos macrófagos com corpos
tingíveis intracitoplasmáticos (restos celulares decorrentes de apoptose). Outra célula
descrita é o centrocito com citoplasma basófilo que contém Ig intracitoplasmática e sintetiza
imunoglobulina (6). As células dendríticas foliculares são observadas somente pela microscopia
eletrônica. Na figura 5 fornecemos as características morfológicas dessas células.
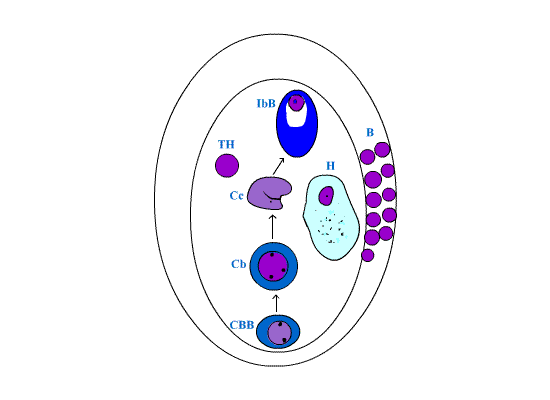
Figura 5: Principais elementos celulares do folículo linfático identificados
através do "imprint" do linfonodo. B = Linfócito B do manto, CBB = Célula blástica
B, Cb = Centroblasto, Cc = Centrocito, TH = Linfócito T auxiliar (T4), IbB = Imunoblasto
B, H = Histiócito com restos celulares.
b) Distribuiįão das células na zona extrafolicular (interfolicular,
paracortical e medular):
Como vimos anteriormente, vamos encontrar nessa região todas as etapas de transformaįão
do linfócito T até imunoblasto e deste até as células efetoras (T4 e T8) e memória. Também
nessa região acontece a ativaįão do linfócito B, responsável pela síntese de IgM, com todas as
etapas de transformaįão até plasmócito e linfócito plasmocitóide passando pelo imunoblasto. A
morfologia dessas células está representada esquematicamente na figura 6.
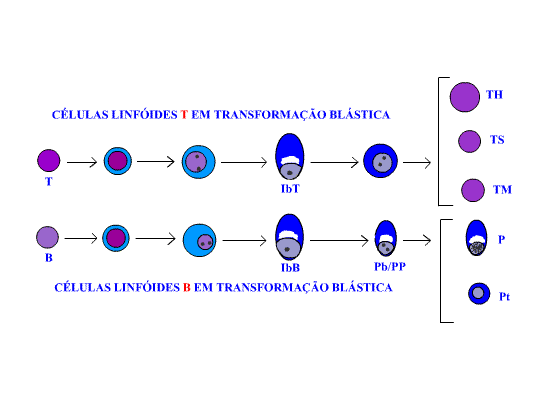
Figura 6: T = Linfócito T, IbT = Imunoblasto T, TH = Linfócito T auxiliar,
TS = Linfócito T supressor, TM = Linfócito T memória, P = Plasmócito, Pt = Linfócito
plasmocitóide, Pb/PP = Plasmablasto/plasmócito, IbB = Imunoblasto B, B = Linfócito B.
Entendemos, pelo exposto, que na zona extrafolicular predominam os pequenos
linfócitos T e B sendo os primeiros em maior número. Entre os linfócitos T, cerca de 60 a 70%
são T4 e o restante T8. As diversas etapas de transformaįão apresentam semelhanįa morfológica,
tanto na B quanto na T, o que impossibilita a distinįão. Somente podemos caracterizar as células
de transformaįão B nas etapas de imunoblasto até a célula efetora, devido ā morfologia típica
da diferenciaįão plasmática (plasmablasto, proplasmócito, plasmócito e linfoplasmocitóide).
Assim, na região extrafolicular, ao contrário da folicular, predominam os pequenos linfócitos,
e a quantidade das células intermediárias (transformadas) ficarão na dependęncia da intensidade
da ativaįão.
Ao examinarmos essa região costumamos anotar a célula que predomina (quase sempre
pequenos linfócitos) e fornecer o grau de transformaįão blástica: discreto, moderado ou
intenso.
O reconhecimento do centro germinativo se dá quando termina a zona de predomínio
dos pequenos linfócitos e surge outra zona com aglomerado de células blásticas (centroblastos)
e de células linfóides maiores que os pequenos linfócitos, com núcleo irregular podendo ter
clivagem, cromatina hipocrômica, nucléolo pouco visível e faixa de citoplasma estreita e pouco
basófilo (centrocitos).
4. Laudo do imprint do linfonodo
Apresentamos no quadro 1 a seqüęncia por nós observada, no exame citológico do imprint
do linfonodo, para orientaįão do laudo.
Conforme mencionamos anteriormente, o estudo citológico do linfonodo pelo imprint serve
para complementar o histopatológico. Desse modo, depois de se diagnosticar uma hemopatia pelo
exame histopatológico, em especial uma síndrome linfoproliferativa, lanįamos mão do imprint para
obter detalhes citológicos, o que facilitará a classificaįão do processo.
Como o processamento do material, para o estudo histopatológico, leva cerca de 2 dias,
e o imprint já pode ser examinado após 30 minutos da realizaįão da biópsia, muitas vezes já
estamos em condiįões de fazer o diagnóstico apenas com esse último procedimento.
O laudo final somente deve ser emitido após estudo conjunto do material pelo corte
histológico (diversas coloraįões, inclusive imuno-histoquímica), imprint (May-Grünwald-Giensa),
suspensão celular e citospin (imuno-citoquímica), e se possível, com as técnicas de
hibridizaįão.
Temos iniciado o tratamento de urgęncia em poucas situaįões, baseados apenas no laudo
pelo imprint, no caso de compressões de vasos sangüíneos, das vias respiratórias, ou do sistema
nervoso (linfoma linfoblástico, tumor de Burkitt) ou no pós operatório imediato (tumor de
Burkitt).
As informaįões fornecidas pelo imprint também são de grande importância para escolher
os anticorpos monoclonais, para a imuno-citoquímica e imuno-histoquímica.
Não devemos desanimar se após o estudo citológico do imprint não chegarmos a uma
conclusão diagnóstica (o que é freqüente). Aguardaremos a conclusão dos demais exames para a
confirmaįão diagnóstica.
Iniciamos o exame procurando observar o tipo de célula predominante. Como é mostrado no
quadro 1, item A, a primeira possibilidade é o predomínio de pequenos linfócitos com
transformaįão blástica pequena ou ausente. Nessa eventualidade, antes de pensarmos em processo
reacional, procuramos afastar a possibilidade de leucemia linfóide crônica. Em se tratando de
crianįa, ou de adulto jovem, esse diagnóstico já é deixado de lado.
Na leucemia linfóide crônica há grande monotonia de pequenos linfócitos (congelamento
em uma etapa da linhagem) e não identificamos centro germinativo. Vamos encontrar, no entanto,
prolinfócitos e linfoblastos (paraimunoblastos), em número variável, na dependęncia dos
subtipos histopatológicos apresentados por Lennert e colaboradores (7): subtipo difuso (7% dos
casos) com pequeno número de prolinfócitos e de linfoblastos dispersos entre os linfócitos;
subtipo pseudofolicular (85% dos casos) com moderado número de prolinfócitos e linfoblastos que
formam aglomerados simulando folículos e o subtipo formado por tumores (8% dos casos) com
grandes aglomerados de prolinfócitos e linfoblastos.
Home | Imprint 1 |
[Imprint 3]




