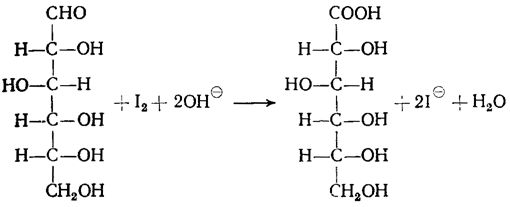
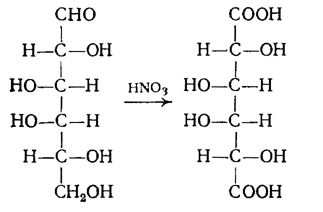
Получение слизевой кислоты из молочного сахара (окисление азотной кислотой).
Осторожно! Выделяются нитрозные газы! Работать под тягой!
0,03 моля молочного сахара растворяют в 120 мл 25%-ной азотной кислоты (d=l,15), упаривают на водяной бане до объема 20 мл, разбавляют 30 мл воды (образующаяся побочно сахарная кислота растворима в воде). Оставляют стоять на несколько дней, затем отсасывают, промывают холодной водой.
Выход 30-40%. Для очистки растворяют в эквивалентном количестве щелочи и осаждают рассчитанным количеством кислоты. Т. пл. 213°С (с разл ).
Получение трихлоруксусной кислоты из хлораля (окисление азотной кислотой).
Осторожно! Трихлоруксусная кислота раздражает кожу: работать в резиновых перчатках! Нитрозные газы: работать под тягой!
В колбе на 250 мл нагревают 0,24 моля хлоральгидрата до плавления и под тягой осторожно прибавляют по каплям 17 мл дымящей азотной кислоты (d=l,5). Когда выделение нитрозных газов начнет ослабевать, смесь нагревают до полного прекращения их выделения, затем перегоняют в вакууме. Т. кип. 102°С (20 мм рт. ст.), т.пл. 57°С; выход 55%.
Полигидроксильные соединения можно в растворах каталитически окислять кислородом на платиновом контакте. При этом наиболее легко окисляется первичная гидроксильная группа, превращаясь в зависимости от условий в альдегидную или карбоксильную. Реакция имеет значение, в частности, при селективном окислении углеводов и их производных, например для получения уроновых кислот.
Получение триметилолуксусной кислоты из пентаэритрита.
[Heyns К, Beck M. Chem. Ber, 1956, 89, 1648.]
В трехгорлой колбе к раствору 7,5 г пентаэритрита в 400 мл воды прибавляют 5г платинового катализатора на угле (приготовление см в разд. Е) и около 10 мл раствора бикарбоната натрия до достижения рН 6,2-6,5. При энергичном перемешивании при 35°С пропускают через раствор в течение 8 ч ток кислорода (~5 пузырьков/с) В ходе реакции, постепенно добавляя раствор бикарбоната натрия, поддерживают рН 6-7 (при отклонении от указанных pH и температуры может происходить более глубокое окисление). За ходом реакции можно следить по расходу щелочи: расход бикарбоната натрия составляет 65% от теоретического. После отфильтровывания катализатора раствор пропускают сначала через ка-тионит (например вофатит KPS или леватит S 100), затем через анионит (вофатит SBK или леватит MN в ОН-форме) С анионита продукт реакции элюиругот, пропуская 150 мл 30%-ной уксусной кислоты, полученный раствор упаривают на водяной бане в вакууме Остаток при охлаждении закристаллизовывается Т.пл 210-213°С (пропанол), выход 50%.
[6.4. Получение хинонов окислением]