[Содержание]
6.3. Окисление первичных и вторичных спиртов и альдегидов
6.3.1. Окисление первичных и вторичных спиртов до альдегидов и кетонов
[6.3.2. Каталитическое дегидрирование первичных и вторичных спиртов до карбонильных соединений]
[6.3.3. Окисление первичных спиртов и альдегидов в карбоновые кислоты]
[6.4. Получение хинонов окислением]
6.3. Окисление первичных и вторичных спиртов и альдегидов
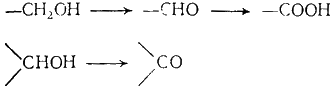 |
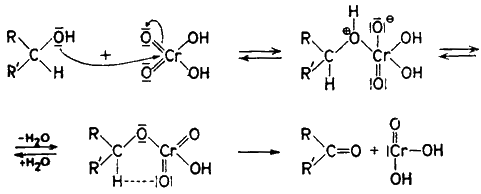
(Г.6.17) |
 |
(Г.6.18) |
| (Г.6.19) |
| n-CH3O > п-трет-С4H9 > п-СН3 > п-Сl > п-NO2 | (Г.6.20) |
| Продукт реакции | Исходное вещество | Т.кип.а, °С | n20D | Выход, % |
| Циклогексанон | Циклогексанол | 155 | 1,4503 | 65 |
| 2-Метилциклогексанон | 2-Метилциклогексанол | 65(23) | 1,4490 | 62 |
| (-)-Ментон | (-)-Ментол | 67(4) [a]20D-29,9° |
1,4536 | 70 |
| цис-Декалон-2 | цис-Декалол-2б | 110(10) | 1,4927 | 60 |
| Этилизопропилкетон | Этилизопропилкарбинол | 112 | 1,3975 | 60 |
| Пропиофенон | Этилфенилкарбинол | 93(11) 21 (т. пл.) |
1,5270 | 65 |
а Цифры в скобках указывают давление (мм рт. ст.), которому соответствует данная температура кипения.
б Можно использовать смесь изомеров, получающуюся при гидрировании (табл 67).
Общая методика окисления вторичных спиртов в кетоны (табл. 86).
[Brown Н. С, Garg С. P. J. Am. Chem. Soc., 1961, 83, 2952].
В трехгорлую колбу на 500 мл, снабженную мешалкой, капельной воронкой, термометром
и обратным холодильником, наливают раствор 0,2 моля соответствующего
спирта в 100 мл эфира. При перемешивании прибавляют в течение 15 мин
раствор 0,067 моля бихромата натрия (при расчете не забывать о кристаллизационной
воде!) и 15 мл серной кислоты в 100 мл воды. Температура реакционной
смеси 25 °С. Перемешивают еще 2 ч при той же температуре, эфирный
слой отделяют, водный еще 2 раза встряхивают с 50 мл эфира. Объединенные
эфирные вытяжки промывают насыщенным раствором бикарбоната натрия,
водой, сушат сульфатом натрия или магния. После отгонки эфира остаток
фракционируют на короткой колонке Вигре.
Методика пригодна для полумикросинтезов: в этом случае удобно применять магнитную мешалку. Окисление можно использовать и для анатптической характеристики вторичных спиртов, переводя неочищенный кетон в подходящие производные.
Нортрицикланон из нортрицикланола путем окисления хромо- вым ангидридом в ацетоне: Meinwald 1., Crandall J., Hymnes W. E. Org. Syntheses. 1965. 45. p. 77.
[6.3.2. Каталитическое дегидрирование первичных и вторичных спиртов до карбонильных соединений]