6. STRUKTURA A VLASTNOSTI KAPALIN
Kapalina se chovají tak, jako by jejich povrch byl pokryt tenkou vrstvou, která se snaží zmenšit plošný obsah povrchu kapaliny. Molekula kapaliny v povrchové vrstvě má vzhledem k sousedním molekulám větší potenciální energii, než by měla, kdyby se nacházela uvnitř kapaliny. Proto má povrchová vrstva povrchovou energii E.
Změní-li se u kapaliny daného objemu její povrch o 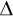 S, změní se její povrchová energie o S, změní se její povrchová energie o
Veloičina  n se nazývá povrchové napětí. Závisí na druhu kapaliny a na prostředí nad volným povrchem kapaliny. S rostoucí teplotou povrchového napětí kapaliny klesá. Jednotkou povrchového napětí je J.m -2. n se nazývá povrchové napětí. Závisí na druhu kapaliny a na prostředí nad volným povrchem kapaliny. S rostoucí teplotou povrchového napětí kapaliny klesá. Jednotkou povrchového napětí je J.m -2.
Síla působící v povrchové vrstvě kapaliny na okraj povrchové blány se nazývá povrchová síla. Její velikost lze vyjádřit ze vztahu
F =  l l,
kde l je délka okraje blány. Z tohoto vztahu vyplívá jednotka povrchového napětí N.m -1.
Vlivem pružných vlastností povrchové vrstvy kapaliny na okraj povrchové kapaliny vzniká pod zakřiveným povrchem kapaliny tzv. kapilární tlak. Pro volný povrch kapaliny kulového tvaru je kapilární tlak dán vztahem
pk = 2 .R -1 .R -1,
kde R je poloměr kulového povrchu a  povrchové napětí. Tenká kulová mýdlová bublina o poloměru R, která má dvě povrchové vrstvy má kapilární tlak určený vztahem povrchové napětí. Tenká kulová mýdlová bublina o poloměru R, která má dvě povrchové vrstvy má kapilární tlak určený vztahem
pk = 4 .R -1 .R -1.
V důsledku kapilárního tlaku pozorujeme v kapilárách kapilární elevaci neboli depresi. V kapiláře vystoupí kapalina do takové výšky h, že hydrostatický tlak odpovídající výšce h je stejný jako kapilární tlak odpovídající zakřivení volného povrchu kapaliny v kapiláře. Tuto podmínku lze napsat ve tvaru
h g = 2 g = 2 .R -1 .R -1,
kde  je hustota kapaliny a R vnitřní poloměr kapiláry. je hustota kapaliny a R vnitřní poloměr kapiláry.
Objem kapaliny se mění s teplotou podle vztahu
V = V1(1 + ß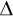 t) t)
a hustota kapaliny podle vztahu
kde ß je součinitel teplotní objemové roztažnosti.
|



