[Содержание]
[6.2. Окисление метильных и метиленовых групп]
6.2.1. Окисление алкиларенов
[6.2.2. Окисление метиларенов до ароматических альдегидов]
6.2.3. Окисление активированных метильных и метиленовых групп в карбонильных соединениях
[6.2.3.1. Окисление двуокисью селена]
[6.2.3.2. Реакция Вильгеродта]
[6.3. Окисление первичных и вторичных спиртов и альдегидов]
6.2.1. Окисление алкиларенов до ароматических карбоновых кислот
В лабораториях для окисления алкиларенов в ароматические карбоновые кислоты еще и сегодня применяют классические окислители: хромовую кислоту (в уксусной или серной кислоте), хромовую смесь, перманганат (обычно щелочной раствор), азотную кислоту, например:
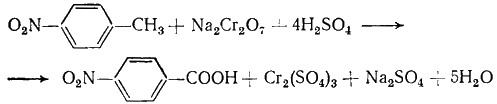 |
(Г.6.7) |
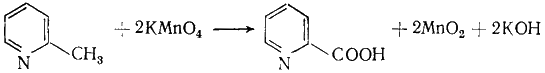 |
(Г.6.8) |
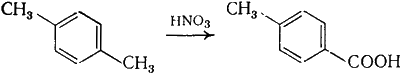 |
(Г.6.9) |
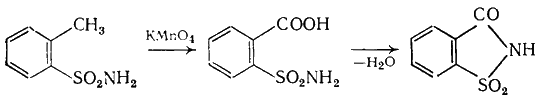 |
(Г.6.10) |
| Конечный продукт | Исходное вещество | Т.пл.,°С | Изоэлектр. точка (рН) | Выход |
| Пиридин-2-карбоновая кислота (пиколиновая кислота) | a-Пиколин | 138 (этанол) | 3,2 | 65 |
| Пиридин-З-карбоновая кислота (никотиновая кислота) | b-Пиколин | 235 (вода) | 3,4 | 73 |
| Пиридин-4-карбоновая кислота (изоникотиновая кислота) | g-Пикoлин | 311 (в запаянном капилляре; вода) | 3,6 | 69 |
Синтез выполняют по методике А (см. выше). Исходят из 0,1 моля сульфонамида и 0,25 моля КМnO4; после подкисления получают сахарин. Выход 50%; т.пл. 228 °С (вода).
Методика окисления пиколинов до пиридинкарбоновых кислот (табл. 81).
[Black О., Depp Е., Corson В. В. J. Org. Chem., 1949, 14, 14].
0,5 моля соответствующего метилпиридина и 500 мл воды нагревают до 70°С
в литровой трехгорлой колбе, снабженной мешалкой, обратным холодильником
и внутренним термометром. При энергичном перемешивании постепенно прибавляют
1,3 моля мелко растертого перманганата калия, разделив его на
10 порций. Очередную порцию вносят после того, как в колбе исчезнет окраска
перманганата от предыдущей порции. Во время добавления первых 5 порций
поддерживают температуру 70°С, затем нагревание ведут на кипящей водяной
бане. После израсходования всего перманганата горячую реакционную смесь
фильтруют при отсасывании, осадок 4 раза промывают горячей водой (порциями
по 100 мл), объединенные фильтраты упаривают в вакууме до объема
~600 мл. Затем к этому раствору прибавляют концентрированную НСl (около
60 мл) до достижения изоэлектрической точки соответствующей пиридинкарбоновой
кислоты, раствор нагревают на кипящей водяной бане и дают медленно
охладиться. Для завершения кристаллизации оставляют раствор с осадком на
ночь в холодильнике; осадок отсасывают, промывают 50 мл холодной воды.
Поскольку пиридин-2-карбоновая кислота (пиколиновая кислота) хорошо растворима в воде (90 г в 100 мл воды при 9°С), то при ее получении раствор перед установлением изоэлектрической точки упаривают до ~200 мл. После этого из двухлитровой трехгорлой колбы, снабженной мешалкой и водоотделителем, добавив 1 л бензола, проводят азеотропную отгонку воды, бензольный раствор фильтруют через воронку для горячего фильтрования, упаривают досуха в слабом вакууме на водяной бане. Регенерированный бензол повторно используют для извлечения пиколиновой кислоты из осадка солей (двухчасовое кипячение), бензольный раствор вновь упаривают и остаток присоединяют к главной массе пиколнновой кислоты.
В промышленности ароматические карбоновые кислоты в больших количествах получают из соответствующих метилбензолов. В качестве окислителей применяют воздух в присутствии пятиокиси ванадия или солей кобальта, а также азотную кислоту.
Таблица 82
| Кислота | Исходное вещество | Т. пл.,°С |
| о-Толуиловая | о-Ксилол | 105 (вода) |
| м-Толуиловая | м-Ксилол | 111 (вода) |
| п-Толуиловая | п-Ксилол | 180 (разб. этанол) |
| 3,5-Диметилбензойная | Мезитилен | 170 (возг.; спирт) |
| п-Хлорбензойная | п-Хлортолуол | 240 (пропанол) |
| Монометиловый эфир терефталевой кислоты | Метиловый эфир п-толуиловой кислоты | 230 (возг., вода) |
Общая методика аутоокисления замещенных в ядре толуолов в соответствующие бензойные кислоты (табл. 82).
[Pritzkow W., частное сообщение.]
В трехгорлую колбу на 500 мл, снабженную
мешалкой, газоподводящей трубкой (рис. 11, а). водоотделителем и обратным
холодильником (Шлифы не смазывать, поскольку смазка действует как ингибитор!
Мешалку смазывать только чистым парафиновым маслом!), помещают 0,5 моля
перегнанного производного толуола, 70 мл
хлорбензола и 0,3-0,5 г стеарата кобальта (см. разд. Е). При окислении
ксилолов и мезитилена загрузку увеличивают до 1 моля, хлорбензол не добавляют.
Через предохранительную склянку (рис. 9), счетчик пузырьков, промывалку
с щелочным раствором КМnО4 и осушительную колонку с КОН в кипящую смесь
пропускают кислород (~30 л в 1 ч). Устанавливают с помощью
реле температуру нагревателя, чтобы обеспечить слабое равномерное кипение;
по ходу реакции нагревание приходится несколько усиливать.
Окисление начинается не позже чем через 2 ч (для инициирования реакции можно добавить 0,1 г азо-бис-изобутиронитрила), в среднем для выполнения синтеза необходимо 6-10 ч. В случае ксилолов реакцию прекращают после того, как в водоотделителе соберется ~5 мл воды. В других случаях окисление ведут до полного прекращения выделения воды. Если выпадающий продукт реакции мешает дальнейшему введению газа, то процесс прерывают, осадок отсасывают, а фильтрат вновь вводят в реакцию.
По окончании реакции смесь оставляют на ночь в холодильнике, осадок отсасывают и перекристаллизовывают. Для регенерации исходного вещества фильтрат перегоняют на колонке. Выход определяют в расчете на израсходованное исходное вещество, он составляет ~50%. С помощью перекристаллизации (из толуола) твердого осадка после перегонки выход можно повысить.
Сведения о техническом применении кислот, получаемых окислением алкиларенов. приведены в табл. 83. В аналогичных условиях в присутствии марганцевых или хромовых катализаторов можно окислять кислородом воздуха алкилбензолы в жидкой фазе до арилалкилкетонов (например, получить ацетофенон из этилбензола).
Таблица 83
| Кислота | Основное применение |
| Бензойная | Консервирующее средство |
| Фталевая (фталевый ангидрид, ср. разд. Г,6.5.1) | ==> Сложные эфиры [средства для отпугивания насекомых (реппеленты), душистые вещества] ==> Oктиловый, бутиловый или этиловый эфиры (пластификаторы) ==> Антрахинон ==> Красители |
| Изофталевая | ==> Алкидные смолы ==> Пластификаторы. |
| Терефталевая | Гликолевый полиэфир терефталевой кислоты (искусственное волокно терилен, гризутен, тревира, дакрон, диолен, лавсан) |
| п-Нитробензойная | ==> п-Аминобензойная кислота ==>Лекарственные препараты [прокаин (новокаин или иенакаин), анестезин] |
| Никотиновая | ==> Амид никотиновой кислоты (витамин) |
| Изоникотиновая | ==> Гидразид изоникотиновой кислоты (INH, неотебен, изониазид, римифон, противотуберкулезный лекарственный препарат) |
В жидкой фазе можно окислить и вторую стоящую у бензольного ядра метильную группу, например, производя аутоокисление в присутствии ацетата кобальта, уксусной кислоты и бромистого водорода получают бензолмонокарбоновые и бензолдикарбоновые кислоты из толуолов и ксилолов: Hay A. S. Blanchard Н. S. Canad. I Chem., 1965, 43, 1306.
[6.2.2. Окисление метиларенов до ароматических альдегидов]