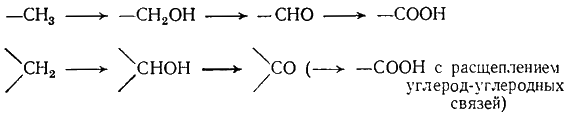
Наряду с этими продуктами в результате множества ионных и радикальных последовательных реакций образуются кетоны, кислоты и другие продукты
окисления. Число их еще более возрастает в результате реакций расщепления
углерод-углеродных связей (см. разд. Г,6.5) и перегруппировок (см. разд. Г,9).
Поэтому окисление предельных углеводородов не может служить методом препаративного получения определенных соединений.
В промышленности же часто является допустимым образование смеси веществ: так, например, при окислении бутана кислородом с ацетатом кобальта
в качестве катализатора при 165 °С под давлением получают смесь продуктов
с примерным соотношением метилэтилкетон : уксусная кислота : метил- и этил-
ацетаты 1 :15 : 3 Промышленное окисление циклогексана в присутствии ацетата кобальта приводит к смеси циклогексанола и циклогексанона (ср.
табл. 68).
Способность алкильной группы к окислению существенно повышается, если она стоит при двойной связи или у ароматического
ядра (ср. разд. Г,1.6). В этих случаях реакция идет существенно
однозначнее (селективнее), образуется меньшее число побочных
продуктов. Конечными продуктами окисления являются карбоновые кислоты, однако, подбирая окислители и условия реакции,
можно получить также альдегиды, а иногда и спирты.
Следует иметь в виду, что активирование метильной или метиленовой группы
олефиновой двойной связью не всегда удается использовать для получения
непредельных карбонильных соединений, так как двойная связь С=С в общем
быстрее поддается действию кислотных окислителей и перманганата калия
(с гидроксилированием и расщеплением углерод-углеродной связи, ср.
разд. Г,4.1.6 и Г,6.5.1), чем алкильная группа. Для подобных селективных
окислений пригодны кислород и двуокись селена (см. разд. Г,6.2.3). Таким
образом, например, в промышленности получают акролеин из пропилена окислением
кислородом в газовой фазе при 350-400°С над катализатором (окись меди).
Акролеин далее через аллиловый спирт превращают в глицерин (см.
разд. Г,4.1.6).
Большое техническое значение имеет окисление углеводородов воздухом в
присутствии аммиака. Так, из метана получают синильную кислоту (метод
Андрусова), из толуола и других метиларенов - бензонитрил и его производные,
из пропилена - акрилонитрил. Последняя из названных реакций представляет
собой в настоящее время наиболее дешевый путь синтеза акрилонитрила (табл. 80).
Таблица 80
Нитрилы, получаемые в промышленности окислительным аммонолизом
| Конечный продукт |
Исходное вещество |
Примечание |
| Синильная кислота |
Метан |
Для сннтезов (см. разд. Г,5.1.7.2 и Г,7.2.1) Инсектофунгицид |
| Акрилонитрил |
Пропилен |
Полиакрилонитрил (ПАН) (см. табл. 53) |
| Бензонитрил |
Толуол |
Средство для набухания ПАН |
| Фталонитрил |
о-Ксилол |
==> Фталоцианины |
| Метакрилонитрил |
Изобутилен |
См. применение метилметакрилата, табл. 53 |
[6.2.1. Окисление алкиларенов]